Warning: Use of undefined constant name - assumed 'name' (this will throw an Error in a future version of PHP) in /home/art6125750/xn--80afieejgglfpb6a5a4k.xn--p1ai/docs/wp-content/themes/twentyseventeen-child/functions.php on line 47
Warning: Use of undefined constant name - assumed 'name' (this will throw an Error in a future version of PHP) in /home/art6125750/xn--80afieejgglfpb6a5a4k.xn--p1ai/docs/wp-content/themes/twentyseventeen-child/functions.php on line 47
Стратегия преодоления и сохранение себя – общие задачи при глаукоме и макулодистрофии
Преодоление специфичной депрессии при диагнозе ВМД означает совершенствование личности и новое самосознание
Продолжим разговор о возрастной макулодистрофии (ВМД) и посмотрим на эту проблему шире, на фоне традиционной проблематики открытоугольной глаукомы и в контексте стратегий адаптации, то есть глазами психолога.
Как известно, жизнь полна неожиданностей, в том числе не самых радостных.
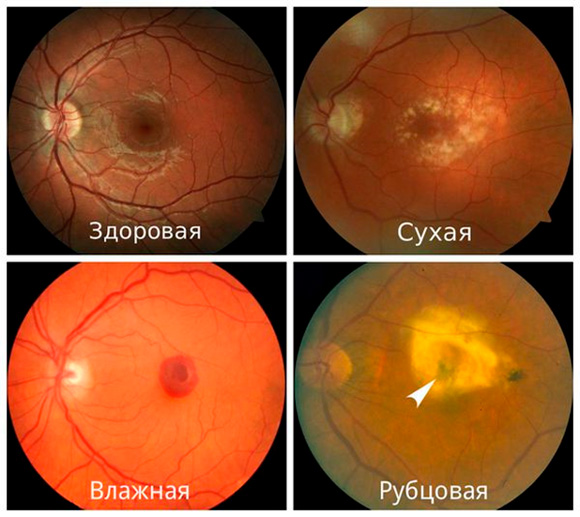
Установлен диагноз возрастной макулодистрофии. Как жить дальше?
Ответ однозначен. Так же, как и после установления диагноза глаукомы: принять, понять, обучаться, адаптироваться, не позволять себя жалеть.

С этих позиций, жизнь с глаукомой и жизнь с макулодистрофией накладывают на человека (чаще всего пожилого) одинаковые обязательства перед собой и своим близким окружением. Возникает аналогичная задача – научиться жить с заболеванием, а для этого научиться его понимать и управлять им по возможности, то есть владеть информацией и применять ее в повседневной жизни.
Безусловно, было бы некорректным сравнивать две тяжелые патологии зрения по сложности и мерам трудностей бытия для заболевшего и его семьи и друзей. У каждого своя клиническая картина течения болезни, свои сопутствующие заболевания, свой психотип, свои жизненные обстоятельства, история семьи. Более того, совершенно необязательно оба заболевания – макулодистрофия и глаукома – диагностируются у одного и того же человека, с разрывом во времени и с одинаковой степенью тяжести течения. Все индивидуально, в том числе так называемая дорожная карта болезни и преодоления.
Общее у данных заболеваний – патологические изменения полей зрения, нейродегенеративный характер поражения глаза, риски для психологического благополучия. Патологические процессы в ходе обоих заболеваний можно тормозить, но макулодистрофия ( в форме, поддающейся лечению) лечится намного труднее и затратнее по сравнению с глаукомой, и протокол лечения не гарантирует успеха, ввиду особенностей течения – разрастания сосудистых новообразований и скопления экссудатов под сетчаткой. С другой стороны, все еще неясны причинно-следственные связи патологий зрения; примером этому – революционная исторически сформированная концепция отечественной офтальмологии о совершенно иной природе повышенного внутриглазного давления и глаукомного процесса.
В первой беседе о макулодистрофии мы обратились к на материалам специализированного целевого фонда The American Macular Degeneration Foundation, AMDF. Здесь детально рассмотрены особенности жизни с возрастной (среднего возраста или ювенальной) макулярной дегенерацией, в том числе психоэмоциональные проблемы. По своей структуре они аналогичны пособиям для больных глаукомой, некоторые образцы которых представлены на нашем сайте.

Помимо традиционного детального ознакомления с сущностью заболевания, пособия AMDF для больных макулодистрофией и их помогающего окружения отличаются усиленным блоком психологических проблем. Это понятно, поскольку психотравма при таком диагнозе тем глубже, чем больше пациент знает о перспективах лечения и шансах на облегчение состояния.
Своего рода инструкция по психологическому сопровождению и поддержанию больного макулодистрофией содержит советы по выстраиванию контактов в общении.
Основной совет по сопровождению касается понимания возникшего дефицита зрения и принятия. Составители пишут: «…Может быть, трудно понять потерю центрального зрения. Может даже показаться, что человек может видеть некоторые вещи, когда хочет. Это связано с тем, что периферийные участки макулы все еще могут работать.
Поговорите терпеливо и мягко с пострадавшим. Постарайтесь понять, как изменилось его зрение и какого рода поддержка ему нужна. Это два вопроса:
1) что именно ты видишь? И что не видишь? Здесь можно помочь, даже просто изменив что-то в привычной обстановке (освещенность, расположение источника света, расположение предметов) и в привычках (книги с более крупным шрифтом).
2) есть ли зрительные галлюцинации (видит предметы, которых нет).
Окажите требуемую организационную или финансовую поддержку в повседневной жизни (оформление документов, покупки продуктов, помощь по дому, оформление социального обслуживания, уход за животными, выбор средств реабилитации для обеспечения безопасного передвижения, перевозка и т. д.).
Выясните настроенность на социальную адаптацию (выбор группы поддержки, сопровождение на встречи).
Эмоциональная поддержка – центральный вопрос нашего материала.

Читаем: «…Опыт жизни с диагностированным заболеванием желтого пятна показывает, что человек проживает эмоциональный кризис, близкий к процессу проживания скорби (горя). Люди могут испытывать последовательно потерю, отрицание, гнев и депрессию до принятия своего состояния. Их личность может измениться. Человек с макулярным заболеванием не будет выглядеть иначе, чем до того, как у него развилось это заболевание. Однако он может быть не в состоянии узнавать друзей и семью. Это может быть неприятно и ему, и окружающим. Некоторые люди с макулярной патологией беспокоятся о том, что они покажутся грубыми, потому что проходят мимо людей, которых знают, не осознавая этого. Людям с макулярным заболеванием часто приходится отказываться от вождения из-за потери зрения.
Эти ограничения могут сильно огорчить, но не обязательно означают конец жизни в социуме. Они по-прежнему могут поддерживать связь со старыми друзьями и даже заводить новых, например, через группы поддержки».
Иногда больной можете чувствовать себя плохо подготовленным, разочарованным, подавленным или испуганным будущим. Эти чувства нормальны. Но ему не нужно справляться в одиночку. В круг поддержки могут входить члены семьи, друзья, ваш врач, другие люди в аналогичной ситуации.
Примечательно, что для людей трудоспособного возраста при наличии у них макулярной болезни предусмотрена специализированная консультационно-информационная служба, которая может ответить на вопросы о жизни с заболеванием желтого пятна. Для пожилых работают как очные, так и онлайн-группы общения и консультаций. Такая же служба работает с родителями детей, имеющих диагноз макулодистрофии. Свои услуги оказывают также родительский форум и самостоятельные службы, разъясняющие особенности образовательной среды для учащихся с данными ограничениями по здоровью.
В Пособии указано, что психологическое сопровождение возрастной группы от 14 до 25 лет с макулодистрофиями имеют свои особенности. Переживания трудностей взросления накладываются на трудности, связанные с дефектом зрения. В результате возможны сильно выраженные стрессовые реакции. Даны ссылки на специализированные центры, куда могут обратиться и учащиеся, и их семьи: Further and higher education; Apprenticeship; Employment and job searching; Welfare benefits; Registration and statutory entitlements; Counselling service for young people over the age of 16; Peer support through Facebook and support groups (то есть группы поддержки со стороны сверстников, в том числе для старших подростков и в социальных сетях). Предлагаются также различные информационные ресурсы, в том числе специальная библиотека и сведения о полезных гаджетах : Information about diagnosis and prognosis; Advice on welfare benefits and employment; Teaching resources for QTVIs; Information on Skills for Seeing and Technology; A library of large print, expert-reviewed information leaflets, to educate and reassure your patients.
Тематический раздел на портале для самообучения и адаптации «Жизнь и самоощущение с AMD» [https://www.macular.org/living-and-thriving-with-amd].
Он включает подразделы
- «Инструменты для жизни» (Вспомогательные технологии для возрастной дегенерации желтого пятна),
- «Эмоциональное благополучие» (о депрессии как естественном состоянии при самостоятельной работе над проблемами ВМД).
- Подраздел «Законодательство и преимущества» разъясняет права пациентов с диагнозом дегенерации желтого пятна с момента постановки диагноза, независимо от тяжести нарушения зрения.
Психиатр Арнольд Вайс (Arnold Wyse, MD), доктор медицины, дает обнадеживающие рекомендации для понимания этого процесса и определения того, когда необходима сторонняя помощь.

Приведем ниже фрагменты из его статьи «Депрессивные состояния у пожилых с макулодистрофией».
«…Депрессивная реакция сопровождается набором типичных физиологических и эмоциональных симптомов. Ее адаптивная функция состоит в том, чтобы сигнализировать человеку о наличии у него важной проблемы, требующей внимания и решения.
Я попытался поставить себя непосредственно на место того, кто испытал такую потерю. Однако вскоре я ощутил, что утрата значительной части столь важного и само собой разумеющегося способа восприятия мира и отношения к нему практически не позволяет мне по-настоящему «знать» ее «изнутри». Возможно, пережить такую потерю, даже в пределах безопасности моего воображения, было просто слишком угрожающе и могло спровоцировать мой собственный болезненный и депрессивный «кризис самости».
То, что действительно сработало на «внутреннем уровне» в этой попытке поместить себя в рамки опыта тех, кто слишком хорошо знает, что такое дегенерация желтого пятна на самом деле, – было волной страха, пробегающей по моему телу и душе (здесь и далее выделено ред.) страх, который разделяют больше людей, чем любой другой страх, связанный с потерей одного из наших пяти чувств, — страх потерять контакт с миром из-за потери зрения.
Ключевой для любой дискуссии о депрессии, вызванной любой провоцирующей причиной, включая дегенерацию желтого пятна, становится «кризис самости», то есть неразрешенный кризис чувства (образа) себя, безопасности и самоуважения.
Когда приходит неожиданный и разрушительный диагноз дегенерации желтого пятна, мир внезапно переворачивается с ног на голову (если только не срабатывает психологическая защита полного отрицания, чтобы избежать эмоциональной боли и защитить привычное представление о себе и чувство безопасности). Даже сочувственные и ободряющие слова врача… часто не могут быть услышаны и эмоционально обработаны в момент постановки диагноза. Ваше восприятие самого себя и видение своего будущего приходят в полный беспорядок; вы в отчаянии представляете себе жизнь во мраке, социальную изоляцию, зависимость, рискованное лечение, потерю друзей, хобби, участия в интересных мероприятиях, таких как спорт, театр, искусство и чтение — короче говоря, своего рода раннюю смерть.
До дегенерации желтого пятна вы уже успешно преодолели кризисы изменений в представлении о себе, которые происходят в средние и более поздние годы жизни, и приняли возможную, но все же в некоторых отношениях отдаленную неизбежность физического упадка. Но теперь это бьет по всем тем же вопросам, только в пиках, и с такой непосредственностью, что настоящее, и особенно будущее, действительно кажется очень «тусклым»…..Ваш безопасный мир рушится, как карточный домик, и ваша самооценка начинает рушиться. с этим.
Один из самых больших страхов и первоначальных ожиданий во время этого процесса «перегруппировки» заключается в том, что человек остается наедине с этой потерей зрения, и что эта потеря будет включать разлуку со значимыми и любимыми людьми. Включение таких людей в выражение утраты и в процесс приспособления заложено в оптимальной исцеляющей функции этого уровня депрессии.
Целью… является не просто возвращение к прежнему уровню функционирования, а процесс обновления личностного роста, который позволит индивидууму достичь большего и более богатого опыта смысла, самооценки, отношений. с другими, и способность справляться с жизненными стрессами, чем это было до травматической потери дегенерации желтого пятна.
NB! Когда обращаться за помощью к психологу или психиатру?
В большинстве случаев в этом нет необходимости, так как возможность «выздоровления» есть у всех, особенно там, где до начала дегенерации желтого пятна существовали прочные межличностные отношения. Однако иногда травматическая ситуация и вытекающая из нее депрессия или тревога, включая озабоченность смертью и самоубийством, становятся настолько подавляющими и затяжными, что показана профессиональная психологическая помощь. Обращение за такой помощью, когда настроение и физические реакции депрессии не исчезли спонтанно, является признаком силы, а не слабости».
Здесь выражена квинтэссенция личностного перерождения в ходе преодоления депрессии после диагноза патологии зрения, и его глубокий смысл.
Полагаем, что эти соображения должны быть на вооружении у всех наших читателей, как больных глаукомой, так и страдающих от иных патологий зрения.
До встречи.







 Третья беседа об этой проблеме посвящена тому, чтобы подчеркнуть, насколько важны для понимания клинической картины глаукомы (точнее, поражений сетчатки) ее ключевые термины и оценочные параметры, и расширить их перечень.
Третья беседа об этой проблеме посвящена тому, чтобы подчеркнуть, насколько важны для понимания клинической картины глаукомы (точнее, поражений сетчатки) ее ключевые термины и оценочные параметры, и расширить их перечень.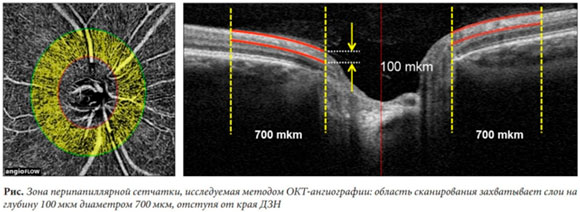
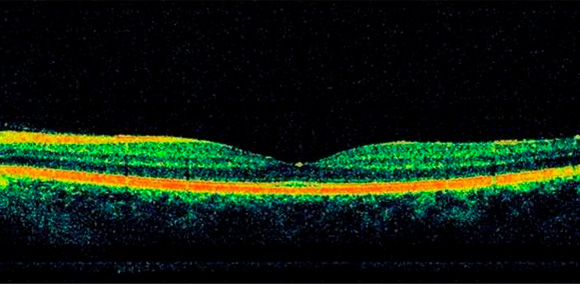
 При этом важны параметры и центральной части сетчатки, и ее периферии.
При этом важны параметры и центральной части сетчатки, и ее периферии. Плексиформный слой – Внутренний сплетениевидный слой (англ. inner plexiform layer, IPL) — один из десяти слоев сетчатки позвоночных и человека, образованный из переплетения аксоновых окончаний биполярных клеток и дендритов амакриновых и ганглионарных клеток.
Плексиформный слой – Внутренний сплетениевидный слой (англ. inner plexiform layer, IPL) — один из десяти слоев сетчатки позвоночных и человека, образованный из переплетения аксоновых окончаний биполярных клеток и дендритов амакриновых и ганглионарных клеток.
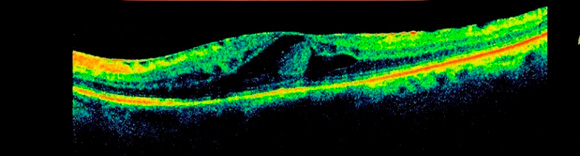
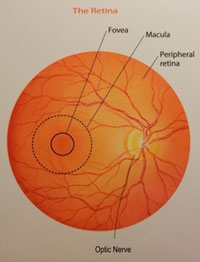 М. подвержена возрастной дистрофии, отекам, разрывам.
М. подвержена возрастной дистрофии, отекам, разрывам.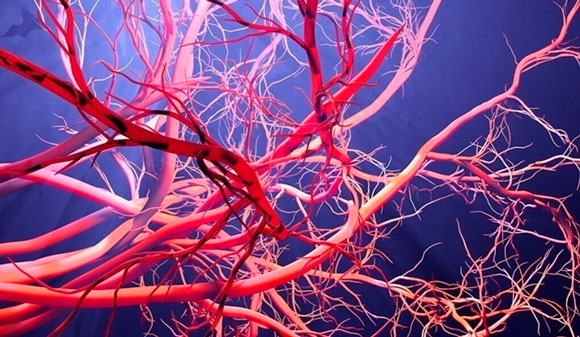
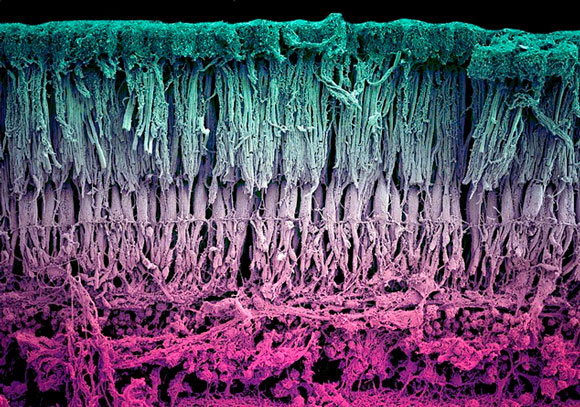
 Свою осторожность в суждениях авторы пояснили следующим образом: «…Выявленное истончение внутренней и наружной сетчатки в фовеальной и парафовеальной областях, а также уменьшение плотности макулярного пигмента могут быть непосредственной причиной снижения световой чувствительности в центральной и парацентральной зонах поля зрения. Однако сами по себе они представляют собой следствие еще не выясненных патологических процессов, захватывающих центральные отделы сетчатки при глаукоме».
Свою осторожность в суждениях авторы пояснили следующим образом: «…Выявленное истончение внутренней и наружной сетчатки в фовеальной и парафовеальной областях, а также уменьшение плотности макулярного пигмента могут быть непосредственной причиной снижения световой чувствительности в центральной и парацентральной зонах поля зрения. Однако сами по себе они представляют собой следствие еще не выясненных патологических процессов, захватывающих центральные отделы сетчатки при глаукоме».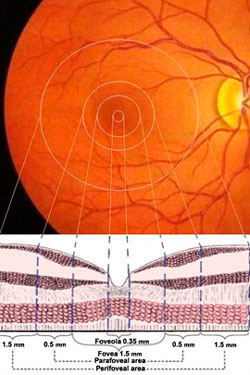 В апреле текущего года American Journal of Ophthalmology разместил онлайн-версию публикации группы офтальмологов клиники Национального Университета Тайваня (Тайбэй) опоискекорреляционнойcвязи состояния микрососудов макулярной зоны, состояния полей зрения и остроты (качества) зрения у больных глаукомой 60-62 лет, находящихся на далеко зашедшей и тяжелой стадии глаукомы и имеющих сравнимый уровень контролируемого внутриглазного давления (около 16 мм.рт.ст.).
В апреле текущего года American Journal of Ophthalmology разместил онлайн-версию публикации группы офтальмологов клиники Национального Университета Тайваня (Тайбэй) опоискекорреляционнойcвязи состояния микрососудов макулярной зоны, состояния полей зрения и остроты (качества) зрения у больных глаукомой 60-62 лет, находящихся на далеко зашедшей и тяжелой стадии глаукомы и имеющих сравнимый уровень контролируемого внутриглазного давления (около 16 мм.рт.ст.).