Warning: Use of undefined constant name - assumed 'name' (this will throw an Error in a future version of PHP) in /home/art6125750/xn--80afieejgglfpb6a5a4k.xn--p1ai/docs/wp-content/themes/twentyseventeen-child/functions.php on line 47
Чудо-микроскоп AOSLO – будущее диагностики и лечения глаукомы
AOSLO позволит оценить реальную эффективность медикаментозного и хирургического лечения и понять принцип действия глазных капель
В Сети размещены как обширная, профессионально изложенная информация по анатомии дренажной сети глаза, так и более понятные непрофессионалу схемы оттока внутриглазной жидкости в норме и патологии (две из них, которые можно увидеть по запросу «трабекулярная сеть», воспроизведены в нашем тексте). Эта многослойная система сложна по строению и до недавнего времени была малодоступна для прямого осмотра и диагностики.
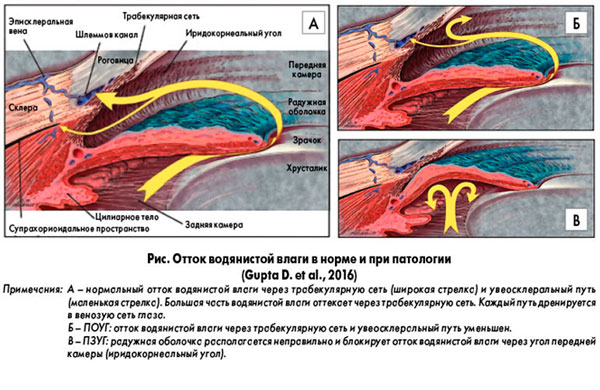
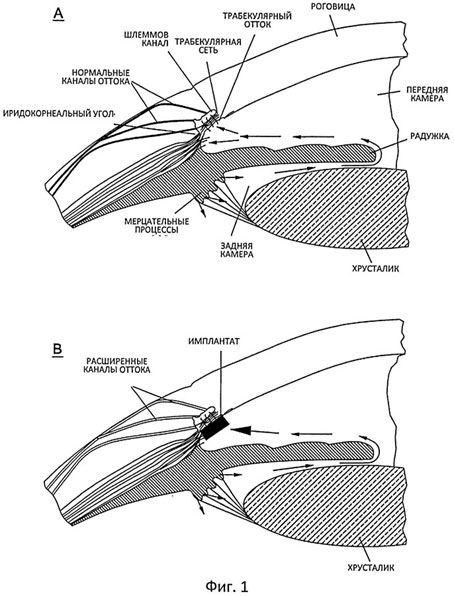
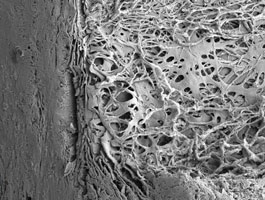
Как видно на этих двух упрощенных рисунках, трабекулярная (дренажная) сеть глаза имеет сложную слоистую (по типу губки) структуру, в которой для выхода внутриглазной жидкости наружу имеются специальные каналы в иридокорнеальном углу (то есть в углу передней камеры, где сходятся роговица и радужка).
 Считается, что клетки дренажной сети одновременно регулируют внутриглазное давление в протоках (канальцах) и работают как фагоцитарные фильтры (поглотители загрязнений), выполняя функцию внутриглазных самоочистителей; это дает нам повод в очередной раз отметить целесообразность и компактность структур и функций замкнутого пространства в биологических системах.
Считается, что клетки дренажной сети одновременно регулируют внутриглазное давление в протоках (канальцах) и работают как фагоцитарные фильтры (поглотители загрязнений), выполняя функцию внутриглазных самоочистителей; это дает нам повод в очередной раз отметить целесообразность и компактность структур и функций замкнутого пространства в биологических системах.
 Для оценки состояния передней камеры глаза у больных глаукомой (и в ходе профилактических осмотров) в традиционной офтальмологии используют гониоскопические линзы (для осмотра передней камеры) в сочетании с осмотром через щелевую лампу. Об этой методике можно прочитать здесь.
Для оценки состояния передней камеры глаза у больных глаукомой (и в ходе профилактических осмотров) в традиционной офтальмологии используют гониоскопические линзы (для осмотра передней камеры) в сочетании с осмотром через щелевую лампу. Об этой методике можно прочитать здесь.
По мере появления высоких технологий стало известно, что выраженная глаукома сопровождается не только гибелью клеток, выстилающих сетчатку (ганглиев), но и механическими повреждениями дренажной трабекулярной сети. Так называемый фиброз клеточного скелета (разрастание соединительной ткани и образование рубцов), распад ферментов, «сшивающих» клетки сети, гибель клеток сетчатки – все эти бедствия приводят к ухудшению качества дренажа внутриглазной влаги, поскольку сеть становится малопригодной для выполнения своей функции очистки и вывода жидкости. Чем меньше и хуже оттекает внутриглазная жидкость, тем выше внутриглазное давление.
Мы в своих публикациях неоднократно писали об этих и других повреждениях на клеточном уровне, характерных для глаукомы (в частности, о разрушении митохондрий, например в http://жизньсглаукомой.рф/act9/, http://жизньсглаукомой.рф/act6/, http://жизньсглаукомой.рф/act3/ ).
Для работы с больными глаукомой и отслеживания клинической картины, особенно при длительном послеоперационном наблюдении в течение нескольких лет, необходима, однако, более детальная информация о состоянии клеток в слоях дренажной системы. Эти перспективы в будущем может обеспечить биомикрогониоскопия, в том случае если новейшие технологии будут доступны для массовых клинических наблюдений и мониторинга глаукомы, как части государственных программ. Иными словами, в будущем необходимо возможно подробнее знать о состоянии тканей в области иридокорнеального угла с помощью так называемого «оптического разреза».
Сегодня постепенно такие возможности открываются. Нам, в частности, удалось прочитать о диагностических возможностях нового прибора для биомикрогониоскопии. И более того – впервые за многолетнюю практику работы с зарубежными научно-практическими публикациями мы увидели в первых абзацах нижеследующей статьи призыв к читателям о сколь возможно быстром распространении содержащейся в статье информации (в переводе или оригинале) среди практикующих офтальмологов.
 В 2019 г. группа оптометристов (специалистов по медицинской оптике) Университета Индианы (США) Brett J. King, Stephen A. Burns, Kaitlyn A. Sapoznik, Ting Luo, and Thomas J. Gast сообщили о разработке и апробации новейшего клинико-диагностического оборудования – адаптивного лазерного сканирующего офтальмо- микроскопа с особо высоким разрешением [adaptive optics scanning laser ophthalmoscope (AOSLO).
В 2019 г. группа оптометристов (специалистов по медицинской оптике) Университета Индианы (США) Brett J. King, Stephen A. Burns, Kaitlyn A. Sapoznik, Ting Luo, and Thomas J. Gast сообщили о разработке и апробации новейшего клинико-диагностического оборудования – адаптивного лазерного сканирующего офтальмо- микроскопа с особо высоким разрешением [adaptive optics scanning laser ophthalmoscope (AOSLO).
Оригинал этой статьи с большим количеством технических описаний и электронных микрофотографий зоны трабекулярной сети можно найти в перечне публикаций журнала Trans Vis Sci Technology за 2019 год на этом сайте (позиция 138).
AOSLO, по утверждениям разработчиков, способен отследить изменение состояния дренажной сети глаза в естественных условиях.
Согласно мнению авторов, AOSLO позволяет на клеточном уровне увидеть состояние трабекулярной сети глаза in vivo (такой, какая она есть в естественных условиях). Поэтапное обследование пациентов с глаукомой на этом приборе позволяет проследить динамику изменений в клеточной структуре с течением времени.
Авторы придают большое значение заявленному ими методу в связи с тем, что появляется возможность на микрометрическом уровне наконец узнать, как же работают капли, предназначенные для снижения внутриглазного давления, какова реальная эффективность лекарственной терапии и хирургических вмешательств (непроникающей склеропластики и введения дренажных имплантов) для того, чтобы затормозить развитие глаукомного процесса.
Авторы вполне логично исходили из того, что внутриглазное давление на сегодня остается единственным измеряемым и изменяемым (динамичным) фактором риска, которым может управлять врач с помощью медикаментозной терапии или хирургического вмешательства.
Исходя из этого принципа, Заявленным новейшим диагностическим признаком глаукомы авторы предлагают считать количество поврежденных клеток одного из слоев клеток эпителия
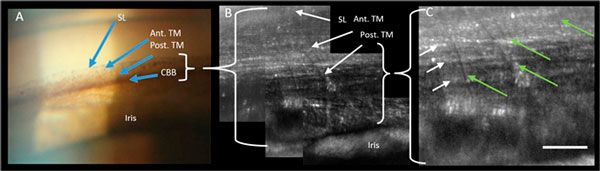
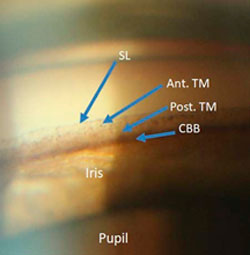 На традиционном гониоскопе с низкой разрешающей способностью врач видит лишь нечеткую слоистую структуру, как видно на микрофотографии из статьи. Как пишут сами авторы, «… при типовом клиническом исследовании угла передней камеры клеточные структуры сети видны только в виде полос, разграниченных пигментацией, и нет их четкой анатомической структуры».
На традиционном гониоскопе с низкой разрешающей способностью врач видит лишь нечеткую слоистую структуру, как видно на микрофотографии из статьи. Как пишут сами авторы, «… при типовом клиническом исследовании угла передней камеры клеточные структуры сети видны только в виде полос, разграниченных пигментацией, и нет их четкой анатомической структуры».
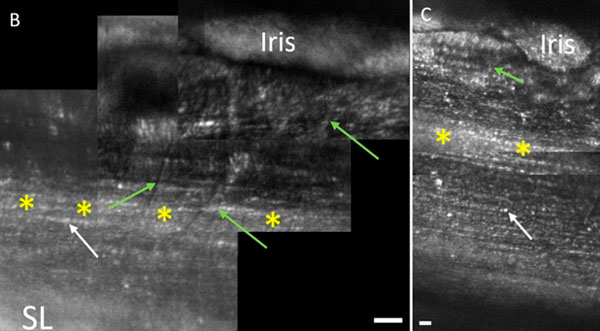
На AOSLO же мы видим другую картину с анатомией слоев: видны «…лучевые сетчатые балки (зеленые стрелки).. и более глубокие, более плотно упакованные пучки корнеосклерального слоя(белые стрелки)». Тем самым возможно выделить для наблюдения практически всю иридокорнеальную область (желтые звездочки). В статье приведено еще несколько сравнительных микрофотографий, сделанных у разных пациентов.
Есть также прямое сопоставление результативности осмотра щелевой лампой и на AOSLO при разном разрешении у одного и того же пациента (см. ниже, обозначения те же).
Итак, усилиями биоинженерии создана диагностическая и клиническая аппаратура следующего поколения, позволяющая в прямом смысле ставить диагноз клеткам тканей глаза.
Остается порадоваться этим достижениям и пожелать следующим поколениям глаукомников испытать на себе эффективность предлагаемого метода диагностики – подсчета поврежденных клеток дренажной сети «по головам».