Авторы
- Казанова С.Ю., врач-офтальмолог высшей категории, заведующая консультативно-диагностическим отделением № 1 (глаукомным отделением);
- Страхов В.В., доктор медицинских наук, профессор, зав. кафедрой офтальмологии.
Первичная открытоугольная глаукома (ПОУГ) относится к социально значимым заболеваниям ввиду её неблагоприятного исхода — необратимой утраты зрительных функций.
Несмотря на значительный прогресс в области фундаментальных исследований глаукомы и технологические достижения, статистика инвалидности и слепоты от глаукомы остаётся удручающей [1-7].
Ранняя диагностика глаукомы позволяет сохранить зрение значительно дольше, чем диагностика заболевания в продвинутой стадии, когда уже наступили необратимые изменения. Не менее важной составляющей является дальнейшее диспансерное наблюдение пациентов [8-11]. Приверженность лечению (комплаенс) всегда выше при острых заболеваниях, сопровождающихся болью, высокой температурой, тяжёлым общим состоянием. Для таких пациентов очевидна как сама необходимость лечения, так и финансовые затраты, окупаемые очевидной положительной динамикой. При хронических заболеваниях — с этим сталкиваются врачи разных специальностей: кардиологи, невропатологи, эндокринологи, др. — пациенты нередко допускают нарушения режима лечения.
Вместе с тем не стоит отрицать ятрогенный фактор в прогрессировании глаукомы. Комплаенс врача (соблюдение стандартов наблюдения и лечения) также влияет на характер течения ПОУГ [12-17].
Таким образом, сохранение зрения при глаукоме зависит от согласованных действий врача и пациента — пациент доверяет свое здоровье профессионалу, будучи обязанным при этом выполнять рекомендации и назначения; врач должен владеть современными знаниями и качественно выполнять свои профессиональные обязанности.
Цель настоящей работы — анализ влияния комплаенса лечения и диспансерного наблюдения (как со стороны пациента, так и со стороны лечащего врача) на скорость прогрессирования глаукомного процесса.
Материалы и методы
Ретрои проспективно проанализировано течение глаукомного процесса 90 пациентов с ПОУГ между двумя визитами в глаукомный центр г. Ярославля. Отбор пациентов осуществлялся при их повторном обращении в 2012-2013 гг. Интервал между посещениями составил от 7 до 117 месяцев, в среднем 41,55 месяца (3,5 года).
Критерии включения в исследование: прогрессирование процесса и снижение зрительных функций между двумя визитами в глаукомный центр.
Критерии исключения:
- аномалии рефракции (миопия, гиперметропия) выше 6,0 дптр, астигматизм выше 3 дптр;
- выраженные помутнения в средах;
- вторичная глаукома;
- закрытоугольная глаукома;
- сосудистая патология глаза (диабетическая ретинопатия, окклюзии сосудов сетчатки, влажная форма макулодистрофии);
- травмы глаза.
Наличие псевдоэксфолиативного синдрома (ПЭС) не являлось критерием исключения, поскольку в отечественной классификации псевдоэксфолиативная глаукома относится к первичной глаукоме [18-20, 33-35].
Все пациенты были разделены на 3 группы по 30 человек в каждой в зависимости от степени приверженности к лечению и качества диспансерного наблюдения.
Первая группа А — нулевой уровень комплаенса пациента. Это те пациенты, кто после первичного обследования и начатого лечения не встали на диспансерный учёт, нигде не наблюдались и не лечились, обратившись повторно уже с жалобами на снижение (или потерю) зрительных функций.
Вторая группа В — недостаточный уровень комплаенса пациента, т. е. пациенты, соблюдавшие лечебный режим не в полном объёме.
Третья группа С — пациенты этой группы выполняли все необходимые рекомендации (в амбулаторных картах не зафиксировано нарушений режима лечения), однако со стороны лечащего врача имело место нарушение стандартов обследования и лечения. Всем пациентам проводили стандартное офтальмологическое исследование — визометрию, периметрию, биомикроскопию, офтальмоскопию, гониоскопию, тонометрию по Маклакову (Рт), пахиметрию (Accupach, «Accutome», США). Исследование полей зрения проводили на приборе Периком (СКТБ «Оптимед», Россия), программа «Глаукома, все точки» (132 стимула). Для удобства восприятия применяли процентное выражение числа скотом. При значительной утрате зрительных функций и эксцентричном (островковом) поле зрения использовали электрический периметр с фиксацией взора пациента на его указательный палец. В этом случае производили расчёт оставшегося поля зрения в градусах и перевод их в проценты (за 100% принято 550°).
Таблица 1
Возрастной и гендерный состав пациентов
|
Группы |
Возраст, лет (М±σ) |
Мужчины, n |
Женщины, n |
|
А |
67,0±10,3 |
18 |
12 |
|
В |
68,3±7,0 |
11 |
19 |
|
C |
64,7±8,8 |
17 |
13 |
|
Всего |
66,7±8,8 |
46 |
44 |
Оптическую когерентную томографию (ОСТ) выполняли на аппарате Cirrus 4000 («Carl Zeiss», Германия). Для анализа использовали показатель толщины слоя нервных волокон (RNFL) как наиболее востребованный в диагностике и мониторинге глаукомы.
Известно, что глаукома является асимметричным заболеванием. Поэтому темпы прогрессирования (переход из одной стадии в другую) оценивались отдельно по худшему и лучшему глазу. Худшим считался глаз с более продвинутой стадией глаукомы, при одинаковой стадии — глаз с более высоким уровнем внутриглазного давления (ВГД) и большей степенью выраженности асимметрии в переднем сегменте и на глазном дне. У 20 пациентов был включён в исследование только один глаз, поскольку парный глаз не имел диагноза глаукомы за период исследования. Таким образом, в исследование были включены 160 глаз (90 худших и 70 лучших).
Стадию глаукомного процесса ставили на основании классификации А.П. Нестерова и А.Я. Бунина [21, 22]. Прогрессирование заболевания оценивали в баллах. Так, переход в следующую стадию (по периметрической симптоматике) был равен прогрессии в один балл. Если происходящие изменения укладывались по полям зрения в рамки одной стадии, но при этом по другим параметрам отмечали отрицательную динамику, шаг прогрессии оценивался в 0,5 балла. Признаки такой динамики: нарастание дистрофических изменений в переднем сегменте глаза, увеличение числа скотом или их депрессия, расширение экскавации, появление кровоизлияний на диске зрительного нерва, уменьшение RNFL.
Обработку полученных данных проводили при помощи прикладных программ MSExcel 2010 для Windows и Statistica 8,0 («Statsoft Inc.», USA).
Из 90 пациентов было 46 мужчин и 44 женщины. Средний возраст при первом обращении составил 66,7 года, группы были сопоставимы по возрасту (табл. 1).
Наследственность является одним из факторов риска возникновения глаукомы. Однако о наличии глаукомы у близких родственников знали менее половины пациентов (36 из 90), возможно, потому, что большинство из них родились в 30-40-е годы XX века — период войн и репрессий, когда связь поколений у многих была оборвана. В то же время факт наличия глаукомы у родственников (и возможные последствия этого заболевания) мог отразиться на последующем режиме диспансерного наблюдения и лечения. Так, в группе A (нулевой уровень комплаенса) имели отягощённую наследственность только 7 пациентов из 30, а в группах А и В — 14 и 15 пациентов соответственно.
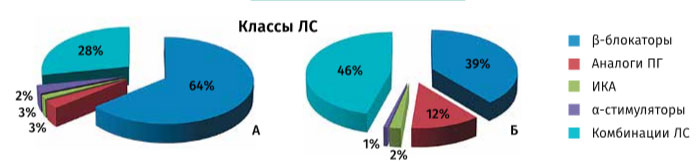
Рис. 1. Медикаментозная терапия глаукомы на первом визите: А — назначения врачей поликлиник; Б — коррекция терапии в глаукомном центре
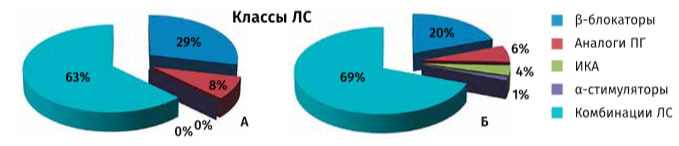
Рис. 2. Медикаментозная терапия глаукомы на втором визите: А — назначения врачей поликлиник; Б — коррекция терапии в глаукомном центре
ПЭС выявлен у 60 (66,7%) пациентов из 90, что подтверждает высокую распространённость данного синдрома в центральной полосе России [23, 24]. Двусторонние клинические проявления ПЭС отмечены у 26 (43,3%) человек из 60. При одностороннем поражении вовлеченность правого и левого глаза составила 35% и 65% соответственно.
Пахиметрия — центральная толщина роговицы (ЦТР) в среднем была равна 539,5±39,6 мкм на худших глазах и 536,5±37,4 мкм на лучших (вариационный ряд от 440 до 645 мкм). Различия по группам были статистически недостоверны (р>0,05).
Результаты
На первом визите в глаукомный центр у 50 пациентов глаукома диагностирована первично. 40 пациентов уже имели стаж заболевания и состояли на диспансерном учёте с глаукомой, 10 из них были оперированы (10 худших и 4 лучших глаза), все операции проникающего типа (синустрабекулэктомия, СТЭК). Лазерная (аргоновая) трабекулопластика (ЛТП) выполнена у одного пациента.
На первый визит в глаукомный центр 53 пациента пришли на консультацию без медикаментозного лечения. Среди лекарственных средств (ЛС), которые были назначены врачами поликлинического звена остальным пациентам (64 глаза), неоспоримое преимущество было за β-блокаторами (рис. 1А).
На рис. 1Б представлены назначения, сделанные врачами глаукомного центра на 1 визите (146 глаз). Мы видим, что при аналогичном выборе препаратов в одном временном интервале спектр назначений существенно отличается — больше назначений из группы аналогов простагландинов (ПГ) и чаще назначаются комбинации ЛС. При этом каждое назначение обсуждалось с пациентами, если финансовых возможностей на длительную дорогостоящую терапию не было, предлагалось оперативное лечение глаукомы.
Все цифры на рисунках по медикаментозному лечению для удобства восприятия переведены в проценты, поскольку число глаз, получающих терапию, на всех визитах было разным.
Уже на первом визите со стороны пациентов было отмечено нарушение лечебного режима — 13 (14%) пациентов из 90 даже не пришли на назначенный контроль ВГД на каплях. И это при том, что на повторный осмотр пациентов записывали через 10-14 дней, оговаривая удобное для них время.
На второй визит 30 пациентов вновь приходят без медикаментозной терапии (все из группы А). Остальные 60 человек (105 глаз) получали лечение, представленное на рис. 2А. В связи с прогрессированием глаукомного процесса схема терапии на этом этапе усложняется, большинству пациентов (63%) врачи назначают несколько препаратов.
В глаукомном центре на втором визите медикаментозное лечение назначается всем пациентам и в худший, и в лучший глаз (n=160). 69% всех назначений — 111 глаз из 160 — составляют различные комбинации ЛС (рис. 2Б).
Появление на фармацевтическом рынке фиксированных комбинаций дало возможность шире использовать сочетания нескольких препаратов из разных классов. Конечно, при подобной терапии комплаенс лечения ниже, чем при закапывании одного препарата один раз в день. Однако при категорическом отказе пациента от операции или противопоказаниях к хирургическому лечению по общему состоянию такая терапия является необходимой (рис. 3).
После проведённого на первом визите обследования и подбора медикаментозного лечения при отсутствии компенсации ВГД принималось решение о лазерном или хирургическом этапе лечения. Проведение ЛТП было рекомендовано 10 пациентам на худший глаз (сделали 8 человек) и 2 пациентам на лучший глаз (сделали оба). На контрольном осмотре через 1 месяц у всех пациентов, прошедших лазерное лечение, было отмечено снижение ВГД до желаемого уровня, и они были направлены по месту жительства на диспансерный учёт.
28 пациентам было рекомендовано хирургическое лечение глаукомы на худший глаз, из них 15 были прооперированы, 13 пациентов отказались или не пришли на госпитализацию. На парный глаз антиглаукомная операция рекомендована в 8 случаях (выполнено 7). Все операции непроникающего типа (непроникающая глубокая склерэктомия, НГСЭ). Далее пациенты уходят на поликлинический этап наблюдения. К сожалению, врачами по месту жительства был упущен второй этап непроникающей хирургии — лазерная десцеметогониопунктура (ДГП).
На втором визите ЛТП применяется реже, поскольку высокий уровень ВГД и продвинутые стадии глаукомы требуют более радикальных мер (хирургического вмешательства). ЛТП была рекомендована в 7 случаях на худший глаз и в 1 случае на лучший. Лазерная ДГП после выполненной ранее НГСЭ рекомендуется 14 пациентам. Учитывая значительную утрату зрительных функций, большинство пациентов сразу переходят на хирургический этап лечения — 58 (!) из 90 пациентов рекомендовано оперативное лечение на худший глаз и в 8 случаях — на лучший глаз. Отказались от оперативного лечения только двое пациентов (в отличие от 1 визита).
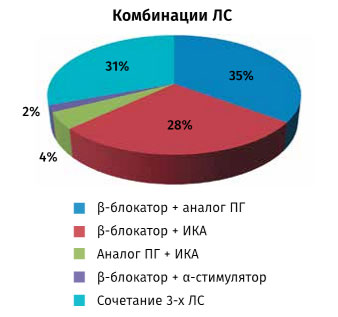
Рис. 3. Сочетания разных классов ЛС в медикаментозной терапии глаукомы (назначения врачей глаукомного центра на втором визите)
Изменилась и хирургическая тактика — по-прежнему преобладает НГСЭ (37 операций), но уже нет 100% выбора хирургов за данный вид вмешательства. Выполнено 27 операций проникающего типа — 24 СТЭК, в трёх случаях имплантирован клапан Ахмеда. В раннем послеоперационном периоде (до 1 месяца после операции) 19 пациентам после НГСЭ выполнена лазерная ДГП.
Стадии заболевания при первом и повторном обращениях представлены на рис. 4.
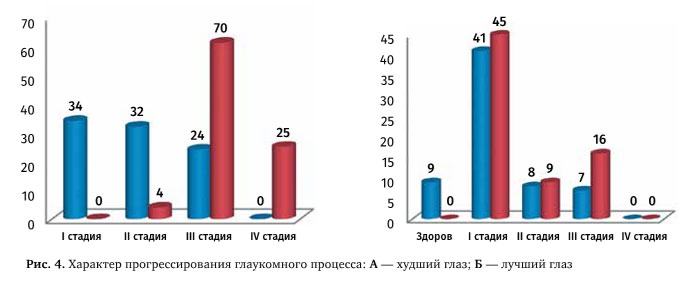
Рис. 4. Характер прогрессирования глаукомного процесса: А — худший глаз; Б — лучший глаз
Таблица 2
Скорость прогрессирования глаукомного процесса в год по группам
|
Группы |
Период между визитами (мес.) | Стадия глаукомы, 1 визит (в баллах) | Стадия глаукомы, 2 визит (в баллах) | Переход по стадиям (Ст2 – Ст1, в баллах) |
КПГ |
|
А |
42,0 |
1,70 |
3,35 |
1,65 |
0,47 |
|
В |
33,83 |
2,07 |
3,30 |
1,23 |
0,44* |
|
C |
46,0 |
1,90 |
3,22 |
1,32 |
0,34** |
|
Среднее |
41,55 |
1,89 |
3,29 |
1,40 |
0,40 |
Примечание: * — р=0,92 в сравнении с КПГ в группе А; ** — р=0,000007 в сравнении с КПГ в группе А, р=0,017 в сравнении с КПГ в группе В.
Как наглядно видно на диаграмме (рис. 4А), на первом визите преобладали пациенты с I–II стадиями глаукомы на худшем глазу, IV стадии глаукомы не было ни у одного пациента. Однако за период между двумя визитами отмечается существенная отрицательная динамика (практически на всех глазах на повторном визите диагностирована III–IV стадия глаукомы). Переход заболевания на одну стадию отмечен на 45 глазах — у каждого второго пациента, на две стадии — на 29 глазах, и даже на три стадии (из I в IV) на 6 глазах. В 10 случаях было ухудшение процесса в пределах одной стадии (отмечена структурная и/или функциональная отрицательная динамика).
На парных глазах за тот же период времени процесс прогрессирования был менее агрессивным, что подтверждает асимметричность течения глаукомы (рис. 4Б) [25]. На 21 глазу из 70 прогрессия не отмечена, на 23 глазах имело место ухудшение течения глаукомы в пределах одной стадии. Переход заболевания на 1 стадию отмечен на 22 глазах, на 2 стадии — на 4 глазах.
Интервал между обращениями: в группе А с нулевым уровнем комплаенса он составил 42,0 мес. Поскольку пациенты этой группы у врача не наблюдались, оценить самостоятельно происходящие изменения они не могли. Поводом для их повторного обращения, как правило, являлось субъективное ощущение снижения зрения, что, к сожалению, означало значительную утрату зрительных функций.
В группе В этот интервал был существенно ниже и составил 33,83 мес. Не соблюдая в полном объёме медикаментозное лечение или нарушая режим посещений, пациенты данной группы всё-таки прислушивались к мнению врача о нестабильности их заболевания и угрозе слепоты. Они наглядно видели эти изменения на распечатках полей зрения, знали уровень своего ВГД, что и заставляло их в конечном итоге пойти на консультацию в глаукомный центр.
Самым высоким интервал между посещениями был в группе C и составил 46,0 мес. Здесь имела место затянутость сроков направления на консультацию со стороны лечащего врача.
Поскольку у всех пациентов был разный временной интервал между посещениями и разные стадии заболевания, нами был разработан специальный показатель — коэффициент прогрессии глаукомы (КПГ), означающий скорость прогрессии за 12 месяцев (календарный год).
Ст2 – Ст1
КПГ = t × 12,
где Ст1 — это стадия глаукомы при первом обращении, выраженная в баллах; Ст2 — стадия глаукомы на втором визите, в баллах; t — интервал между визитами (месяцы).
Таким образом, проведённый анализ показал, что при несоблюдении режима лечения и наблюдения (как со стороны пациента, так и со стороны врача) скорость прогрессии глаукомного процесса на худшем глазу крайне высока и составляет в среднем 0,40 балла в год. Это означает переход заболевания на 1 стадию за 2,5 года в среднем по всем группам (табл. 2).
При этом темпы прогрессии были достоверно выше в группах А и В и ниже в группе С. Иными словами, при отсутствии лечения от первой стадии глаукомы до терминальной проходит в среднем 6 лет, при несоблюдении пациентом режима наблюдения и лечения — 7 лет, при несоблюдении стандартов лечения лечащим врачом — 9 лет.
Скорость прогрессирования глаукомного процесса на лучших глазах оказалась значительно ниже — КПГ составил в среднем 0,17 балла в год, другими словами, переход заболевания на одну стадию происходит на парном глазу за 6 лет.
Динамику функциональных нарушений оценивали по данным периметрии и она представлена на рис. 5.
При анализе функциональных нарушений обнаружена выраженная отрицательная динамика полей зрения по худшему глазу — за период между посещениями глаукомного центра процент абсолютных скотом увеличился с 17 до 50 (в 3 раза). Данные изменения не могли быть не замечены пациентами, что и заставило их обратиться на повторную консультацию.
Динамику, происходящую в слое нервных волокон сетчатки (по данным ОСТ), оценить во всей группе не представлялось возможным, поскольку первый визит многих пациентов приходился на тот период, когда на базе глаукомного отделения прибора для данного исследования не было. В свою очередь, из тех пациентов, кому ОСТ была выполнена при первом обращении, в ряде случаев на втором визите уже не было возможности выполнить контрольное исследование (из-за низкой остроты зрения в IV стадии).
Только у 15 пациентов ОСТ выполнена при первом и втором посещениях. Если рассматривать динамику по худшему глазу, из них на первом визите 10 пациентов имели II стадию глаукомы и 5 пациентов — I стадию (по периметрической симптоматике). На втором визите на всех глазах зафиксирована III стадия. Интервал между обследованиями в среднем составил 30,2 мес. Отмечена отрицательная динамика толщины RNFL у всех 15 пациентов — с 68,4 мкм на первом визите до 54 мкм на втором, что подтверждает прогрессирование глаукомного процесса. Структурные нарушения сопровождались функциональными.
Внутриглазное давление (ВГД), его превышение толерантных для конкретного пациента зна чений и суточные колебания являются факторами риска развития и прогрессирования глаукомы [26-30, 36-40]. В нашей работе ВГД также было главным повреждающим фактором, вызывая структурные и функциональные изменения.
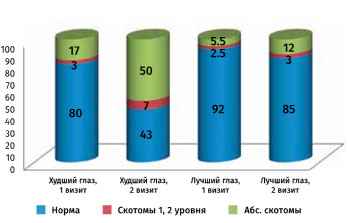
Рис. 5. Динамика изменений полей зрения между двумя визитами в глаукомный центр
Как видно из табл. 3, после подобранного на первом визите лечения удалось достичь значительного снижения ВГД (в среднем на 33% от исходного уровня). У 13 пациентов оценить ВГД после лечения не удалось, поскольку они не явились на контрольный приём. Однако через несколько лет все пациенты приходят на второй визит с таким же высоким давлением, как при своём первом обращении, в группе А уровень ВГД был даже выше исходного (р=0,0079). Снижение ВГД на втором визите после коррекции лечения (преимущественно хирургического) составило 41%, однако зрительные функции у большинства пациентов были необратимо утрачены.
Таблица 3
Уровень ВГД в группах А, В, С на первом и втором визитах до и после коррекции лечения, худший глаз
Примечание: * — р=0,0079 в сравнении с исходным уровнем ВГД на первом визите (группа А).
|
Группы |
ВГД (Рт), мм рт.ст. |
|||
|
1 визит (n=90) |
после коррекции лечения (n=77) |
2 визит (n=90) |
после коррекции лечения (n=90) | |
|
Группа А |
34,57 | 21,91 |
39,43* |
22,89 |
|
Группа В |
32,17 | 23,48 |
32,26 |
20,03 |
|
Группа С |
32,66 | 21,28 |
31,27 |
18,03 |
|
Среднее |
33,13 | 22,18 |
34,32 |
20,23 |
Таблица 4
Уровень ВГД в группах на лучших глазах
|
ВГД (Рт), мм рт.ст. |
||||
|
1 визит (n=70) |
после коррекции лечения (n=59) |
2 визит (n=70) |
после коррекции лечения (n=70) | |
|
Среднее |
25,76* |
21,25 |
26,23** |
20,90 |
Примечание: * — р<0,00001 в сравнении с ВГД худшего глаза на первом визите; ** — р<0,00001 в сравнении с ВГД худшего глаза на втором визите.
В группе А ВГД на втором визите было достоверно выше, чем в группах В и С (р=0,0003 и р=0,00003 соответственно). Быстрый распад зрительных функций пациентов этой группы был связан с постоянно повышенным до высоких цифр уровнем ВГД, нарастающим с течением времени. Однако в группах В и С уровень ВГД на втором визите достоверно не отличался (р=0,415), при этом скорость прогрессии в этих группах была разной — достоверность различий КПГ р=0,017 (табл. 2). Вероятно, высокая скорость прогрессии у недостаточно комплаентных пациентов была обусловлена не только субкомпенсированным уровнем ВГД, но и колебаниями давления, связанными со систематическими пропусками закапывания.
Прогрессирование глаукомного процесса на парных глазах было менее агрессивным, поскольку ВГД на момент обращения пациентов было достоверно ниже, чем на худших глазах (табл. 4). Скорректированное на первом визите лечение позволило понизить ВГД на 17,5% от исходного уровня, но этот результат был нивелирован ко второму визиту. Снижение ВГД на втором визите составило 20,3%.
Заключение
В результате исследования темпов прогрессирования глаукомного процесса в группах с различными вариантами некомплаентности лечения было установлено, что в среднем переход заболевания на одну стадию происходит за 2,5 года на худшем глазу. Это выше, чем в ряде других исследований [31, 32, 41-45], поскольку в ретроспективные анализы, проводимые по диспансерным картам поликлинических учреждений, по-видимому, не попадают пациенты с нулевым уровнем комплаенса (группа А). Они встают на диспансерный учёт только при повторном обращении, соответственно, период отрицательной динамики глаукомного процесса таких пациентов оказывается вне статистической обработки.
На парном глазу скорость прогрессии ниже и составляет одну стадию в 6 лет. С одной стороны, это подчёркивает асимметричность течения глаукомы, с другой — свидетельствует о том, что на парных глазах мы диагностируем заболевание раньше и лечим его активнее (а пациент лучше выполняет наши рекомендации), имея в качестве отрицательного примера худший глаз.
Темпы прогрессирования были выше в группах А и В (нарушение режима лечения пациентами) и ниже в группе С (тактика врача). Однако скорость прогрессии в группе С также была достаточно высокой, что говорит о равной ответственности обоих участников лечебного процесса.
Литература / References
- Leske M.C. The epidemiology of POAG: a review. Am J Epidemiol
- Quigley H.A. Number of people with glaucoma worldwide. Br J Ophtalmol 1996; 80(5):389-393.
- Quigley H.A., Broman A.T. The number of people with glaucoma worldwide in 2010 and 2020. Br J Ophtalmol 2006; 90(3): 262-267.
- Волков В.В. Как диагностировать и контролировать начальную открытоугольную глаукому. Глаукома 2009; 2:3-13. [Volkov V.V. How to diagnose and control early open-angle glaucoma. Glaucoma 2009; 2:3-13. (In Russ.)].
- Волков В.В. Глаукома открытоугольная. Москва: МИА, 2008; 352 с. [VolkovV.V. Glaukoma otkrytougolnaya [Open-angle glaucoma]. Moskow: MIA, 2008; 352 p. (In Russ.)].
- Либман Е.С. Эпидемиологическая характеристика глаукомы. Глаукома 2009; 1 (приложение): 2-3. [Libman E.S. Glaucoma epidemiological characteristic. Glaucoma 2009; 1 (Suppl.): 2-3. (In Russ.)].
- Шараф Важди Мохамед, Сипливый В.И. Эпидемиологические особенности клинического течения глаукомы в зависимости от социальных, экономических, этнических и географических факторов. Национальныйжурналглаукома2014; 1:68-76. [Charaf W.M., Siplivy V.I. Epidemiological aspect of glaucoma clinical progression, depending on social, economic, ethnic and geographic factors. Natsional’nyi zhurnal glaucoma 2014; 1:68-76. (In Russ.)].
- Романова Т.Б., Романенко И.А. Диспансеризация глаукомы: прошлое и настоящее. Клиническая офтальмология 2007; 2:75-78. [Pomanova T.B., Romanenko I.A. Clinical examination of glaucoma. Clin Ophtalmology 2007; 2:75-78. (In Russ.)].
- Шиловских О.В., Стренёв Н.В., Пасенова И.Г. Оценка состояния диспансеризации больных глаукомой на примере крупного промышленного центра. Глаукома. Журнал НИИ ГБ РАМН 2013; 1:24-27. [Shilovskikh O.V., Strenev N.V., Pasenova I.G. Estimation of glaucoma patients monitoring through the example of a big industrial city. Glaukoma. Zhurnal NII Glaznyh Bolezney RAMN 2013; 1:24-27. (In Russ.)].
- Мачехин В.А., Фабрикантов О.Л. К вопросу о раннем выявлении и диспансеризации больных глаукомой. Практическая медицина. Офтальмология 2013; 70(1-3):44-47. [Machekhin V.A., Phabrikantov O.L. On early detection and medical examination of patients with glaucoma. Practical medicine. Ophthalmology 2013; 70(1-3):44-47. (In Russ.)].
- Догадова Л.П., Жаров В.В., Амиров А.Н. Ранее выявление, скрининг, мониторинг и диспансеризация больных глаукомой. В кн.: Глаукома. Национальное руководство. Под ред. Е.А. Егорова. Москва: ГЭОТАР-Медиа, 2013; 780-818 с. [Dogadova L.P., Zharov V.V., Amirov A.N. Rannee vyyavlenie, skrining, monitoring i dispanserizatsiya bol’nykh glaukomoj. V kn. pod red. Egorov E.E.: Glaukoma. Natsional’noe rukovodstvo [Early detection, screening, monitoring and clinical examination of glaucoma patients. In: Egorov E.E., editors. Glaucoma. National leadership]. Moscow: GEOTAR-Media, 2013; 780-818 p. (In Russ.)].
- Алексеев В.Н., Малеванная О.А. О качестве диспансерного наблюдения при первичной открытоугольной глаукоме. Клиническая офтальмология 2003; 3:119-122. [Аlekseev V.N., Malevannaya O.А. On the quality of follow-up in primary open-angle glaucoma. Clinical Ophthalmology 2003; 3:119-122. (In Russ.)].
- Алексеев В.Н., Малеванная О.А., Тубаджи Ессам, Никитин Д.Н., Газизова И.Р. Прогрессирующая глаукома — неизбежность или недоработка? Глаукома.ЖурналНИИГБРАМН 2012; 3:26-31. [Alekseev V.N., Malevannaya O.A., Nader Samih ElHaj, Nikitin D.N., Gazizova I.R. Progressive glaucoma – inevitability or incomplete treatment? Glaukoma. Zhurnal NII Glaznyh Bolezney RAMN 2012; 3:26-31. (In Russ.)].
- Бикбов М.М., Бабушкин А.Э., Мурова Л.Х., Матюхина Е.Н. Результаты диспансерного наблюдения и поликлинического этапа лечения больных первичной открытоугольной глаукомой. Глаукома. Журнал НИИ ГБ РАМН 2012; 4:31-35. [Bikbov M.M., Babushkin A.E., Murova L.H., Matuyhina E.N. Results of case followup and out-patient phase of primary open-angle glaucoma patients treatment. ZhurnalNII Glaznyh Bolezney RAMN 2012; 4:31-35. (In Russ.)].
- Кунин В.Д., Редид А.А. Эффективность длительной диспансеризации больных первичной открытоугольной глаукомой. Глаукома. Журнал НИИ ГБ РАМН 2012; 4:18-23. [Kunin V.D., Redid A.A. Effectiveness of long term follow-up of primary openangle glaucoma patients. Glaukoma. Zhurnal NII Glaznyh Bolezney RAMN 2012; 4:18-23. (In Russ.)].
- Казанова С.Ю., Страхов В.В. Комплайнс. Взгляд на проблему с другой стороны. Глаукома. Журнал НИИ ГБ РАМН 2012; 3:58–60. [Kazanova S.Yu., Strakhov V.V. Compliance. A look at the problem from another angle. Glaukoma. Zhurnal NII Glaznyh Bolezney RAMN 2012; 3:58-60. (In Russ.)].
- Казанова С.Ю., Страхов В.В. Сравнительная оценка качества лечения первичной открытоугольной глаукомы. Российский офтальмологический журнал 2013; 4:92-95. [Kazanova S.Y., Strakhov V.V. Comparative evaluation of the quality of treatment of primary open-angle glaucoma. RussianOphthalmologicalJ 2013; 4:92-95. (In Russ.)].
- Егоров Е.А., Астахов Ю.С., Щуко А.Г. Национальное руководство (путеводитель) по глаукоме для поликлинических врачей. Москва: Столичный бизнес, 2008; 136 с. [Egorov E.A., Astakhov Yu.S., Shcuko A.G. Natsional’noe rukovodstvo po glaukome dlya praktikuyushhikh vrachei [National glaucoma guidance for clinic doctors]. Moscow: Capital business, 2008; 136 p. (In Russ.)].
- Национальное руководство по глаукоме для практикующих врачей. 2-е изд. Под ред. Е.А. Егорова, Ю.С. Астахова, А.Г. Щуко. Москва: ГЭОТАР-Медиа, 2011; 280 с. [Egorov E.A., Astakhov Yu.S., Shuko A.G., editors. Natsional’noe rukovodstvo po glaukome dlya praktikuyushhikh vrachej. 2-e izd. [National guidance on glaucoma for medical practitioners. 2nd ed.]. Moscow: GEOTAR-Media, 2011; 280 p. (In Russ.)].
- Национальное руководство по глаукоме для практикующих врачей. 3-е изд. Под ред. Е.А. Егорова, Ю.С. Астахова, А.Г. Щуко. Москва: ГЭОТАР-Медиа, 2015; 454 с. [Egorov E.A., Astakhov Yu.S., Shuko A.G., editors. Natsional’noe rukovodstvo po glaukome dlya praktikuyushhikh vrachej. 3-e izd. [National guidance on glaucoma for medical practitioners. 3nd ed.]. Moscow: GEOTAR-Media, 2015; 454 p. (In Russ.)].
- Нестеров А.П. Глаукома. Москва: МИА, 2008; 357 с. [Nesterov A.P. Glaukoma [Glaucoma]. Moskow: MIA, 2008; 357 p. (In Russ.)].
- Нестеров А.П. Первичная глаукома. Москва: Медицина, 1982; 288 с. [Nesterov A.P. Pervichnaya glaucoma [Primary glaucoma]. Moskow: Meditsina Publ., 1982; 288 p. (In Russ.)].
- Курышева Н.И., Брежнев А.Ю., Гапкова С.Г. Распространенность псевдоэксфолиативной глаукомы в Центральном и Центрально-Черноземном регионах России. Глаукома 2008; 3:11-15. [Kurysheva N.I., Brezhnev A.Yu., Kapkova S.G. The prevalence of pseudoexfoliative glaucoma in the Central and Central-Chernozem regions of Russia. Glaucoma 2008; 3:11-15. (In Russ.)].
- Баранов В.И., Брежнев А.Ю. Псевдоэксфолиативный синдром в Центральной России: клинико-эпидемиологическое исследование. Российский офтальмологический журнал 2012; 1:22-24. [Baranov V.I., Brezhnev A.Yu. Pseudoexfoliation syndrome in Central Russia: a clinical and epidemiological study. Russian Ophthalmological J 2012; 1:22-24. (In Russ.)].
- Страхов В.В., Алексеев В.В., Ермакова А.В., Корчагин Н.В., Казанова С.Ю. Асимметрия тонометрических, гемодинамических и биоретинометрических показателей парных глаз в норме и при первичной глаукоме. Глаукома 2008; 4:11-16. [Strakhov V.V., Alekseev V.V., Ermakova A.V., Korchagin A.V., Kazanova S.Yu. Asymmetry of tonometric, hemodinamic and byoretinometric parameters of twin eyes in healthy patients and in primary glaucoma. Glaucoma 2008; 4:11-16. (In Russ.)].
- Нестеров А.П., Бунин А.Я., Кацнельсон Л.А. Внутриглазное давление. Физиология и патология. Москва: Наука, 1974; 384 с. [Nesterov A.P., Bunin A.Ya., Katsnelson L.A. Vnutriglaznoe davlenie. Fiziologiya i patologiya [Intraocular pressure. Physiology and pathology]. Moskow: Nauka Publ., 1978; 384 p. (In Russ.)].
- Алексеев В.Н., Егоров Е.А., Мартынова Е.Б. О распределении уровней внутриглазного давления в нормальной популяции. РМЖ. Клиническая офтальмология 2001; 2:38-40. [Alexeev V.N., Egorov E.A., Martinova E.B. On the distribution of intraocular pressure levels in the normal population. RMJ. Clinical Ophthalmology 2001; 2:38-40. (In Russ.)].
- Балалин С.В., Фокин В.П. О роли внутриглазного давления в диагностике и лечении первичной открытоугольной глаукомы. РМЖ. Клиническая офтальмология 2010; 4:113-115. [Balalin S.V., Fokin V.P. On the role of intraocular pressure level in diagnostics and treatment of POAG. RMJ. Clinical Ophthalmology 2010; 4:113-115. (In Russ.)].
- Петров С.Ю., Антонов А.А., Макарова А.С., Вострухин С.В. Офтальмотонус в оценке медикаментозного и хирургического лечения глаукомы. РМЖ. Клиническая офтальмология 2015; 2:69-72. [Petrov S.Yu., Antonov A.A., Makarova A.S., Vostrukhin S.V. Intraocular pressure in assessment of medical and surgical treatment of glaucoma. RMJ. Clinical ophthalmology 2015; 2:69-72. (In Russ.)].
- Куроедов А.В., Брежнев А.Ю., Александров А.С. Как понизить уровень внутриглазного давления на 30% у пациентов с глаукомой (обзор литературы). Военно-медицинский журнал 2009; 330(6):40-46. [Kuroyedov A.V., Brezhnev A.Yu., Alexandrov A.S. Principles of ocular pressure reduction by 30% in patients with glaucoma (Review of literature). Voenno-meditsinskii zhurnal 2009; 330(6):40-46. (In Russ.)].
- Нероев В.В., Киселева О.А., Бессмертный А.М. Основные результаты мультицентрового исследования эпидемиологических особенностей первичной открытоугольной глаукомы в Российской Федерации. Российский офтальмологический журнал 2013; 3:4-7. [Neroev V.V., Kiseleva O.A., Bessmertny A.M. The main results of a multicenter study of primary open-angle glaucoma epidemiological features in the Russian Federation. Russian Ophthalmological J 2013; 3:4-7. (In Russ.)].
- Егоров Е.А., Алексеев В.Н., Куроедов А.В. Эпидемиология глаукомы в Российской Федерации. В кн.: Глаукома. Национальное руководство. Под ред. Е.А. Егорова. Москва: ГЭОТАРМедиа, 2013; 44-62 с. [Egorov E.E., Alekseev V.N., Kuroedov A.V. Epidemiologiya glaukomy v Rossijskoj Federatsii. V kn. рod red. E.E. Egorov: Glaukoma. Natsional’noe rukovodstvo [Epidemiology of glaucoma in the Russian Federation. In: E.E. Egorov, editors. Glaucoma. National leadership]. Moscow: GEOTAR-Media, 2013; 44-62 p. (In Russ.)].
- Щуко А.Г., Юрьева Т.Н., Чекмарева Л.Т., Малышев В.В. Редкие формы глаукомы. Иркутск, 2002. [Shchuko A.G., Yur’eva T.N., Chekmareva L.T., Malyshev V.V. Redkie formy glaukomy [Rare forms of glaucoma]. Irkutsk, 2002. (In Russ.)].
- Щуко А.Г., Юрьева Т.Н., Чекмарева Л.Т., Малышев В.В. Глаукома и патология радужки. Москва, 2009. [Shchuko A.G., Yur’eva T.N., Chekmareva L.T., Malyshev V.V. Glaukoma i patologiya raduzhki [Glaucoma and iris pathology]. Moscow, 2009. (In Russ.)].
- Брежнев А.Ю., Курышева Н.И., Трубилин В.Н., Баранов В.И. Проблемы ранней клинической диагностики псевдоэксфолиативного синдрома. Офтальмология 2012; 9(1):49-52. [Brezhnev A.Yu., Kurysheva N.I., Trubilin V.N., Baranov V.I. Problems of early clinical diagnostics of the pseudoexfoliation syndrome. Ophthalmology 2012; 9(1):49-52. (In Russ.)].
- Еричев В.П., Козлова И.В., Макарова А.С., Цзинь Д. Особенности системной гемодинамики у больных первичной открытоугольной глаукомой, компенсированным внутриглазным давлением и нестабилизированным течением. Национальный журнал глаукома 2013; 3:20-23. [Erichev V.P., Kozlova I.V., Makarova A.S., Jin Dan. Features of systemic hemodynamics in patients with progressive primary open-angle glaucoma with compensated intraocular pressure. Natsional’nyi zhurnal glaukoma 2013; 3:20-23. (In Russ.)].
- Петров С.Ю., Антонов А.А., Макарова А.С., Вострухин С.В. Офтальмотонус в оценке медикаментозного и хирургического лечения глаукомы. РМЖ. Клиническая офтальмология 2015; 16(2):69-72. [Petrov S.Yu., Antonov A.A., Makarova A.S., Vostrukhin S.V. IOP in the assessment of medical and surgical treatment of glaucoma. RMJClinicalOphthalmology2015; 16(2):69-72. (In Russ.)].
- Щуко А.Г., Юрьева Т.Н. Алгоритмы диагностики и лечения больных первичной глаукомой. Иркутск, 2009. [Shchuko A.G., Yur’eva T.N. Algoritmy diagnostiki i lecheniya bol’nykh pervichnoi glaukomoi [Algorithms for diagnosis and treatment of patients with primary glaucoma]. Irkutsk, 2009. (In Russ.)].
- Шмырева В.Ф., Петров С.Ю., Антонов А.А., Данилов С.С. Исследование суточных колебаний офтальмотонуса у пациентов с первичной открытоугольной глаукомой при монотерапии тимололом, латанопростом и травопростом. РМЖ. Клиническая офтальмология 2010; 11(4):125-127. [Shmyreva V.F., Petrov S.Yu., Antonov A.A., Danilov S.S. The study of daily IOP fluctuations in primary open-angle glaucoma patients with timolol, latanoprost and travoprost monotherapy. RMJ Clinical Ophthalmology 2010; 11(4):125-127. (In Russ.)].
- Куроедов А.В., Еричев В.П., Ходыкина Н.П., Городничий В.В. и др. О корреляционных взаимоотношениях между суточными колебаниями внутриглазного давления и морфометрической структурой диска зрительного нерва. Офтальмология 2006; 3(1):43-49. [Kuroedov A.V., Erichev V.P., Khodykina N.P., Gorodnichii V.V. et al. On the correlation relationship between daily intraocular pressure fluctuations and morphometric structure of the optic nerve. Ophthalmology 2006; 3(1):43-49. (In Russ.)].
- Куроедов А.В., Авдеев Р.В., Александров А.С., Бакунина Н.А. и др. Первичная открытоугольная глаукома: в каком возрасте пациента и при какой длительности заболевания может наступить слепота. Медико-биологическиепроблемы жизнедеятельности 2014; 2(12):74-84. [Kuroedov A.V., Avdeev R.V., Aleksandrov A.S., Bakunina N.A. et al. Primary open-angle glaucoma: at which age and disease duration can blindness occur. Medicalandbiologicalproblemsof life 2014; 2(12):74-84. (In Russ.)].
- Авдеев Р.В., Александров А.С., Бакунина Н.А., Басинский А.С. и др. Модель манифестирования и исходов первичной открытоугольной глаукомы. Клиническая медицина 2014; 92(12): 64-72. [Avdeev R.V., Aleksandrov A.S., Bakunina N.A., Basinskii A.S. et al. Model of primary open-angle glaucoma manifestation and outcomes. Clinical medicine 2014; 92(12):64-72. (In Russ.)].
- Авдеев Р.В., Александров А.С., Бакунина Н.А., Басинский А.С. и др. Прогнозирование продолжительности сроков заболевания и возраста пациентов с разными стадиями первичной открытоугольной глаукомы. Национальный журнал глаукома 2014; 13(2):60-69. [Avdeev R.V., Aleksandrov A.S., Bakunina N.A., Basinskii A.S. et al. Prediction of the disease duration and the age of patients with different stages of primary open-angle glaucoma. Natsional’nyi zhurnal glaukoma 2014; 13(2):60-69. (In Russ.)].
- Куроедов А.В., Авдеев Р.В., Александров А.С., Бакунина Н.А. и др. Предполагаемый возраст пациентов и период болезни для проведения интенсивных лечебно-профилактических манипуляций при первичной глаукоме. ОфтальмологияВосточная Европа 2014; 22(3):60-71. [Kuroedov A.V., Avdeev R.V., Aleksandrov A.S., Bakunina N.A. et al. The estimated patient age and disease stage for intensive treatment in primary glaucoma. Ophthalmology Eastern Europe 2014; 22(3):60-71. (In Russ.)].
- Астахов Ю.С., Рахманов В.В. Наследственность и глаукома. Офтальмологические ведомости 2012; 4:51-57. [Astakhov Yu.S., Rakhmanov V.V. Heredity and glaucoma. Ophthalmologicheskiye vedomosti 2012; 4:51-57. (In Russ.)].