Авторы
- Светикова Л.А., к.м.н., врач-офтальмолог;
- Иомдина Е.Н., д.б.н., профессор, главный научный сотрудник отдела патологии рефракции, бинокулярного зрения и офтальмоэргономики;
- Игнатьева Н.Ю., д.х.н., доцент кафедры физической химии химического факультета;
- Серик А.Н., к.м.н, начальник офтальмологического центра;
- Мигаль С.Ф., заведующий офтальмологическим отделением;
- Иванченко О.В., врач лабораторной диагностики;
- Назарова Н.А., врач-офтальмолог.
Как показывают исследования последних лет, состояние соединительнотканной (корнеосклеральной) оболочки глаза играет существенную роль в развитии и прогрессировании первичной открытоугольной глаукомы (ПОУГ) [1-6].
При этом патологические изменения склеры пациентов с ПОУГ не соответствуют, как это предполагалось ранее [7-12], ускоренному процессу старения и не укладываются в рамки естественных геронтологических особенностей этой ткани, поскольку при развитии ПОУГ в склере выявляются специфические структурные нарушения и формируются избыточные сшивки коллагеновых структур ферментативной природы, а не вызванные процессами гликации (как при старении) [13, 14].
Известно, что с возрастом обмен веществ, в том числе и в соединительной ткани, замедляется, растет количество внутрии межмолекулярных сшивок коллагеновых структур, сформированных неферментативным путем (гликация), и увеличивается содержание зрелых коллагеновых волокон [15].
Однако в склеральной ткани пациентов с ПОУГ происходит не только избыточное накопление белков и уплотнение внеклеточного матрикса, в том числе за счет увеличения количества сшивок коллагена, сформированных путем гликации, но и, по-видимому, усиливаются процессы ферментативного сшивания за счет активации трансглутаминазы [16], как это происходит в трабекулярной ткани [17].
Кроме того, показано, что в тканях и средах глаз пациентов с ПОУГ нарушен баланс между матричными металлопротеиназами, отвечающими за распад коллагеновых волокон, и их ингибиторами [18-22]. Возможно, такой дисбаланс наблюдается и в глаукомной склере, что приводит к накоплению в ней зрелого коллагена [1, 15].
Для оценки уровня сшитости коллагеновых волокон и содержания фибриллярного коллагена в настоящее время используют метод дифференциальной сканирующей калориметрии (ДСК). ДСК позволяет определить температуру и теплоту конформационного перехода «спираль-клубок» данного белка.
Термомеханическая стабильность коллагена, характеризующаяся показателем температуры денатурации (Тд), существенно зависит от посттрансляционной модификации макромолекул коллагена, от упаковки макромолекул в фибриллы, волокна и пучки, а также от взаимодействия коллагена с другими матриксными макромолекулами, которое осуществляется путем формирования внутрии межмолекулярных поперечных сшивок. Термически индуцированные трансформации коллагена, включающие, в том числе, распад сшивок, отражают общее исходное состояние коллагеновой структуры [23-26].
У пациентов с ПОУГ повышена Тд и энтальпия (теплота) денатурации (ΔHm) склеры, что свидетельствует о ее повышенной сшитости и накоплении в ней коллагена [1]. Эти показатели увеличиваются по мере прогрессирования процесса, при этом даже на I стадии глаукомы показатели выше, чем у пациентов того же возраста без глаукомы [14].
Возможно, при ПОУГ изменяется состояние коллагена не только склеры, но и других соединительнотканных структур организма, как это отмечается, например, при миопии [27]. Установлено, что при прогрессировании миопии уменьшается биомеханическая стабильность корнеосклеральной оболочки, а также нарушается обмен веществ в соединительной ткани организма в целом.
У детей и подростков с миопией чаще выявляются биомеханические нарушения опорно-двигательного аппарата (плоскостопие, сколиоз, гастроптоз, гипермобильность суставов и другие) [28]. При этом в другой соединительнотканной оболочке миопического глаза — теноновой капсуле — так же, как и в склере, уменьшается количество сшивок коллагена, снижается диаметр коллагеновых фибрилл, что свидетельствует об общем нарушении стабильности соединительнотканных структур миопического глаза [29].
В недавней работе приводятся данные о том, что в теноновой капсуле пациентов с ПОУГ наблюдаются качественно те же структурно-механические изменения, что и в склеральной оболочке глаукомного глаза [30]. О возможном наличии соединительнотканных нарушений в организме пациентов с ПОУГ свидетельствует совместное исследование тайваньских и японских ученых, которое показало, что у пациентов с пролапсом митрального клапана, вызванным дезорганизацией соединительной ткани, чаще развивается ПОУГ [31].
В то же время сведений о том, вовлекается ли соединительная ткань придаточного аппарата глаза больных с ПОУГ в патологический процесс, характерный для соединительнотканных структур глаукомного глаза, в доступной литературе мы не нашли. Цель настоящей работы — изучение особенностей состояния коллагеновых структур придаточного аппарата глаза у пациентов с ПОУГ.
Материалы и методы
У 12 пациентов, проходивших лечение в офтальмологическом центре 3 ЦВКГ им. А.А. Вишневского, в ходе хирургических вмешательств были взяты 17 образцов различных тканей: 13 образцов кожи века 8 пациентов при блефаропластических операциях, 3 образца хряща 3 пациентов в ходе хирургического устранения выворота века, 1 образец склеры у 1 пациента на этапе выполнения непроникающей глубокой склерэктомии. Возраст пациентов составил от 55 до 87 лет (медиана 71 год). При этом 7 образцов тканей взяты у пациентов с ПОУГ II и III стадий и 10 — у пациентов без глаукомы.
Всем пациентам выполнялось стандартное офтальмологическое обследование (визометрия, биомикроскопия, рефрактометрия, офтальмоскопия, пневмотонометрия, гониоскопия, периметрия). После антиглаукоматозной операции формирование вновь созданных путей оттока отслеживали с помощью тонометрии, оптической когерентной томографии (ОСТ) переднего отрезка на томографе RTVue-100 («Optovue», США) и фоторегистрации фильтрационной подушки.
Для оценки уровня поперечной связанности коллагена оценивали термомеханические показатели исследуемых образцов ткани с помощью современного высокотехнологичного метода дифференциальной сканирующей калориметрии (ДСК) на аппарате Phoenix DSC 204 («Netzsch», Германия). Определяли термодинамические параметры денатурации коллагена образцов склеры, кожи и хряща век: эндотермический температурный пик — Тд (°С) и энтальпию — ΔHд (Дж/г сухого веса).
Таблица 1
Медианы ΔHд (Дж/г сухого веса) и Тд (°С) образцов кожи век и хряща у пациентов различного возраста с ПОУГ и без ПОУГ
|
Вид ткани |
Средний возраст (медиана), лет |
ΔHд |
Тд |
| Кожа пациентов без ПОУГ |
57 |
7,03 |
66,6 |
| Кожа пациентов без ПОУГ |
75 |
9,12 |
67,25 |
| Кожа пациентов с ПОУГ |
74 |
9,33 |
67,35 |
| Хрящ пациентов без ПОУГ |
71 |
8,26 |
66,6 |
| Хрящ пациентов с ПОУГ |
78 |
10,10 |
67,1 |
Результаты
В табл. 1 представлены результаты определения ΔHд и Тд образцов исследованных тканей.
Как показывают данные, приведенные в табл. 1, ΔHд и Тд кожи века у пациентов в возрасте 55-60 лет (медиана — 57 лет) ниже, чем у пациентов 72-79 лет (медиана — 75 лет), что свидетельствует о возрастном увеличении уровня поперечной связанности и накоплении коллагена в этой структуре придаточного аппарата глаза. У пациентов с ПОУГ той же возрастной группы (медиана — 74 года) данные показатели кожи века выше, чем у здоровых пациентов.
Термомеханические показатели хряща век пациентов близкого возраста (71-78 лет) без ПОУГ и с ПОУГ также оказались различными (см. табл. 1): аналогично коже века, коллаген хряща века глаз с ПОУГ характеризуется более высоким уровнем поперечной связанности.
Наличие связи уровня поперечной связанности коллагена кожи век и склеры глаукомного глаза иллюстрирует следующий клинический пример.
У пациента К., 72 года, с диагнозом: ПОУГ II а правого глаза, ПОУГ III а левого глаза, начальная катаракта обоих глаз, — были взяты образцы кожи век правого и левого глаза при выполнении блефаропластики. ΔHд и Тд кожи века правого и левого глаза составили 9,97 Дж/г и 66,3°С, 13,1 Дж/г и 66,4°С соответственно, при этом показатель ΔHд кожи века левого глаза (с более продвинутой, чем на правом глазу, стадией ПОУГ) оказался существенно выше возрастной нормы (см. табл. 1).
Через 6 месяцев пациенту на левом глазу была выполнена непроникающая глубокая склерэктомия в связи с нестабильным течением глаукомы на максимальном гипотензивном режиме. Показатели ΔHд и Тд склеры составили 4,8 Дж/г и 65,9°С, что несколько выше, чем средний показатель Тд, соответствующий этой стадии ПОУГ (Tд =64,2±2,0°С) [1].
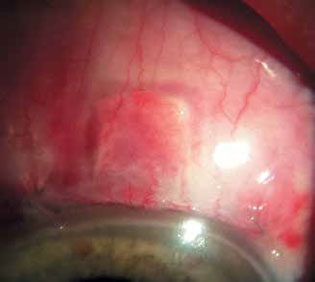
Рис. 1. Фильтрационная подушка в день операции
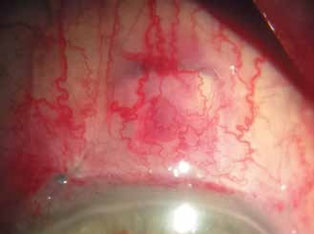
Рис. 2. Фильтрационная подушка на 5-й день после операции
Вид фильтрационной подушки в день операции представлен на рис. 1.
В дальнейшем отмечена тенденция к рубцеванию, уплощение подушки, расширение сосудов на 5-й день после операции (рис. 2). ВГД на оперированном глазу составило 18 мм рт.ст.
Пациенту выполнен массаж фильтрационной подушки. ВГД снизилось до 15 мм рт.ст. Затем массаж фильтрационной подушки выполнялся на профилактических осмотрах пациента (примерно 1 раз в 5 дней). ВГД выше 19 мм рт.ст. зафиксировано не было. На контрольном осмотре через 1 месяц ВГД 22 мм рт.ст. Фильтрационная подушка представлена на фото (рис. 3) и ОСТ-сканограмме (рис. 4).
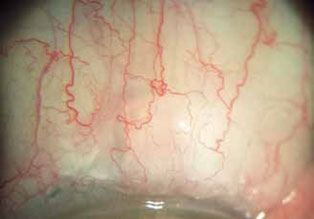
Рис. 3. Фильтрационная подушка через 1 месяц после операции
По результатам ОСТ полости в субконъюнктивальном пространстве практически отсутствуют, при этом в интрасклеральном пространстве определяется зона уменьшенной оптической плотности, что может свидетельствовать о развитии склероконъюнктивального сращения. В связи с этим пациенту выполнен нидлинг фильтрационной подушки с 0,4% раствором дексаметазона 0,2 мл. ВГД нормализовано. Через 1,5 месяца после операции на ОСТ определяются полости в субконъюнктивальном и интрасклеральном пространстве (рис. 5). ВГД составило 18 мм рт.ст. без гипотензивного режима.
В течение всего срока наблюдения пациента (1,5 года) ВГД не поднималось выше 18 мм рт.ст. без гипотензивного режима, зрительные функции стабильны. На рис. 6 и 7 представлены фото фильтрационной подушки через 12 и 18 месяцев соответственно.
Обсуждение
В ходе исследования мы выявили, что с возрастом показатели Тд и ΔHm тканей придаточного аппарата глаза (кожи и хряща век) закономерно увеличиваются, что соответствует естественному для процесса старения накоплению коллагена и росту количества сшивок коллагеновых структур соединительной ткани. В то же время обнаруженное увеличение показателей Тд и ΔHm у пациентов с ПОУГ по сравнению с соответствующими показателями пациентов той же возрастной группы без ПОУГ может свидетельствовать о специфических изменениях соединительной ткани придаточного аппарата глаза, по-видимому, аналогичных изменениям склеры глаукомных глаз.
Сравнение термомеханических показателей кожи века правого и левого глаза пациента К. наталкивает на мысль о возможной зависимости структуры соединительной ткани придаточного аппарата глаза от стадии глаукомы. На правом глазу пациента, где имеется II стадия ПОУГ, ΔHд и Тд (9,97 Дж/г и 66,3°С) ниже, чем на левом глазу (13,1 Дж/г и 66,4°С), но судить о взаимосвязи тяжести глаукомного процесса и состояния коллагена тканей придаточного аппарата глаза на основании сравнения двух глаз одного и того же пациента, безусловно, неправомочно.
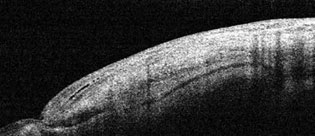
Рис. 4. ОСТ-сканограмма фильтрационной подушки через 1 месяц после операции
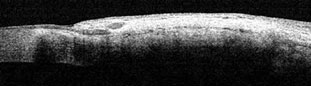
Рис. 5. ОСТ-сканограмма фильтрационной подушки через 1,5 месяца после операции
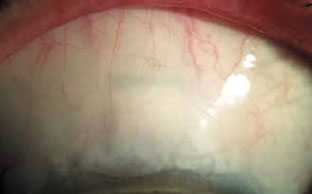
Рис. 6. Фильтрационная подушка через 12 месяцев после операции
На примере того же пациента можно также сопоставить имеющееся увеличение поперечной связанности и уровня коллагена склеры (что свидетельствует о наличии дисбаланса между синтезом и распадом этого белка) с процессом формирования вновь созданных путей оттока внутриглазной жидкости после антиглаукоматозной операции. Тд образца склеры левого глаза этого пациента составила 65,9°С при среднем значении Тд для III стадии глаукомы, равном 64,2±2,0°С, полученном нами в более ранних исследованиях [1].
Это может свидетельствовать о выраженном нарушении метаболизма соединительнотканной оболочки у данного пациента, в частности, о преобладании процессов синтеза коллагена над его распадом. Данное утверждение опосредованно подтверждается течением послеоперационного периода после антиглаукоматозной операции: развитием избыточного рубцевания, нарушением функционирования вновь созданных путей оттока и необходимостью применения дополнительной терапии (нидлинга) для стабилизации состояния и повышения эффективности хирургического лечения.
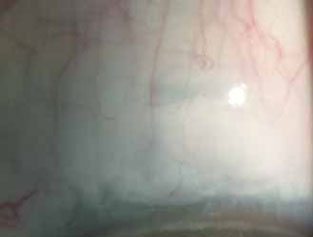
Рис. 7. Фильтрационная подушка через 18 месяцев после операции
На сегодняшний день выполнена первая часть ДСК-исследования тканей придаточного аппарата глаза и склеры, которая позволила выявить определенные закономерные тенденции. Очевидно, данные исследования целесообразно продолжить для получения достоверных корреляционных зависимостей термомеханических показателей тканей век от наличия и степени тяжести глаукомного поражения.
Заключение
В работе выявлена отчетливая тенденция к увеличению поперечной связанности коллагена и его количества в тканях век (кожи и хряща) с возрастом, при этом у пациентов с ПОУГ эти показатели оказались выше, чем у лиц той же возрастной группы без глаукомы. Подобные изменения были выявлены нами ранее в склере у пациентов разного возраста с ПОУГ.
Таким образом, полученные результаты позволяют сделать вывод о возможном соответствии у пациентов с ПОУГ изменений структуры и свойств соединительной ткани в оболочках глаза и его придаточного аппарата.
Литература / References
- Иомдина Е.Н., Игнатьева Н.Ю., Данилов Н.А., Арутюнян Л.Л., Киселева О.А., Назаренко Л.А. Биохимические и cтруктурнобиомеханические особенности матрикса склеры человека при первичной открытоугольной глаукоме. Вестник офтальмологии 2011; 6:10-14. [Iomdina N., Ignatieva N.Yu., Danilov N.A., Arutunyan L.L., Kiseleva O.A., Nazarenko L.A. Biochemical, structural and biomechanical features of human scleral matrix in primary openangle glaucoma. Vestn Oftalmol 2011; 6:10-14. (In Russ.)].
- Страхов В.В., Алексеев В.В. Патогенез первичной глаукомы — все или ничего. Глаукома 2009; 2:40-52. [Strakhov V., Alekseev V.V. The pathophysiology of a primary glaucoma —«all or nothing». Glaucoma 2009; 2:40-52. (In Russ.)].
- Светикова Л.А., Иомдина Е.Н., Киселева О.А. Биомеханические и биохимические особенности корнеосклеральной капсулы глаза при первичной открытоугольной глаукоме. Российский офтальмологический журнал 2013; 2:105-110. [Svetikova A., Iomdina E.N., Kiseleva O.A. Biomechanical and biochemical parameters of the corneoscleral capsule of patients with primary openangle glaucoma. Russian Ophthalmological J 2013; 2:105-110. (In Russ.)].
- Quigley A., Cone F.E. Development of diagnostic and treatment strategies for glaucoma through understanding and modification of scleral and lamina cribrosa connective tissue. Cell Tissue Res 2013; 353(2):231–244. doi: 10.1007/s00441-013-1603-0.
- Jones J., Girard M.J., White N., Fautsch M.P., Morgan J.E., Ethier C.R., Albon J. Quantitative analysis of three-dimensional fibrillar collagen microstructure within the normal, aged and glaucomatous human optic nerve head. J R Soc Interface 2015; 12(106). doi: 10.1098/rsif.2015.0066.
- Tamm R., Braunger B.M., Fuchshofer R. Intraocular pressure and the mechanisms involved in resistance of the aqueous humor flow in the trabecular meshwork outflow pathways. Prog Mol Biol Transl Sci 2015; 134: 301-14. doi: 10.1016/bs.pmbts.2015.06.007.
- Нестеров А.П. Глаукома. М.: Медицина, 1995; 256 с. [Nesterov P. Glaucoma [Glaucoma]. Moscow, Meditsina Publ., 1995: 256 p. (In Russ.)].
- Затулина Н.И., Панормова Н.В., Сеннова Л.Г. Концепция патогенеза первичной открытоугольной глаукомы. В кн.: VII Съезд офтальмологов России. М., 2000; 1:131. [Zatulina I., Panormova N.V., Sennova L.G. The conception of primary openangle glaucoma. In: Proc. of VII All-Russian ophthalmological congress. Moscow; 2000; 1:131. (In Russ.)].
- Затулина Н.И. Сравнительное морфологическое изучение дренажной системы глаза при физиологическом старении и первичной глаукоме. В кн.: Морфологические основы клинической и экспериментальной офтальмологии. Москва; 1978: 17-18. [Zatulina I. Comparative study of the eye drainage system in physiological aging and in primary glaucoma. In: Morphological basis of clinical and experimental ophthalmology. Moscow; 1978: 17-18. (In Russ.)].
- Светлова О.В., Кошиц И.Н. Старение оболочек глаза — возможное ключевое звено в патогенезе открытоугольной глаукомы. В кн.: VII съезд офтальмологов России. Москва; 2000; 1:193. [Svetlova V., Koshitz I.N. Aging of eye coats — possible cue chain in the pathogenesis of primary open angle glaucoma. In: Proc. of VII All-Russian ophthalmological congress. Moscow; 2000; 1:131. (In Russ.)].
- Кошиц И.Н., Светлова О.В., Котляр К.Е. и др. Биомеханический анализ традиционных и современных представлений о патогенезе первичной открытоугольной глаукомы. Глаукома 2005; 1:41-62. [Koshitz N., Svetlova O.V., Kotliar K.E. et al. Biomechanical analysis of traditional and contemporary conceptions on pathogenesis of the primary open-angle glaucoma. Glaucoma 2005; 1:41-62. (In Russ.)].
- Симановский А.И. Сравнительный анализ изменения биомеханических свойств склеры в процессе естественного старения и при развитии глаукоматозной патологии. Глаукома 2005; 4:13-19. [Simanovsky A.I. Comparative analysis of the changing of sclera biomechanical properties in the process of natural aging and in glaucoma development. Glaucoma 2005; 4:13-19. (In )].
- Иомдина Е.Н., Игнатьева Н.Ю., Арутюнян Л.Л. и др. Изучение коллагеновых и эластических структур склеры глаз при глаукоме с помощью нелинейно-оптической (мультифотонной) микроскопии и гистологии (предварительное сообщение). Российский офтальмологический журнал 2015; 8(1):50-56. [Iomdina N., Ignatieva N.Yu., Arutunyan L.L., et al. A study of collagen and elastin structures of the sclera in glaucoma using nonlinear optical (multiphoton) microscopy and histology, a preliminary report. Russian Ophthalmological J 2015; 8(1):50-56. (In Russ.)].
- Иомдина Е.Н., Арутюнян Л.Л., Игнатьева Н.Ю. Сравнительное изучение возрастных особенностей уровня поперечной связанности коллагена склеры пациентов с различными стадиями первичной открытоугольной глаукомы. Российский офтальмологический журнал 2016; 9(1):20-28. [Iomdina Е.N., Arutyunyan L.L., Ignatieva Yu. A comparative study of agerelated level of sclera collagen crosslinking in patients with different stages of primary open-angle glaucoma. Russian Ophthalmological J 2016; 9(1):20-28. (In Russ.)].
- Fratzl Collagen. Structure and Mechanics. Potsdam, Springer, 2008: 506 p.
- Данилов Н.А., Игнатьева Н.Ю., Иомдина Е.Н. и др. Исследование склеры глаукомных глаз с помощью физико-химического анализа. Биофизика 2011; 56(3):520-526. [Danilov A., Ignatieva N. Yu., Iomdina E.N., et al. Sclera of the glaucomatous eye: physicochemical analysis. Biophysics 2011; 56(3):520-526. (In Russ.)].
- Welge-Lussen , May C.A. Induction of tissue transglutaminase in the trabecular meshwork by TGF-betal and TGF-beta2. Invest Ophthalmol Vis Sci 2000; 41(8):2229-2238.
- Agapova O.A., Ricard C.S., Salvador-Silva M., Hernandez R. Expression of matrix metalloproteinases and tissue inhibitors of metalloproteinases in human optic nerve head astrocytes. Glia 2001; 33(3):205-216.
- Ashworth Briggs L., Toh T., Eri R., Hewitt A.W., Cook A.L. TIMP1, TIMP2, and TIMP4 are increased in aqueous humor from primary open-angle glaucoma patients. Mol Vis 2015; 21:1162-1172.
- Avila G., Ginebra M., Hayakawa T. et al. Collagen metabolism in human aqueous humor from primary open-angle glaucoma. Arch Ophthalmol 1995; 113:1319-1323.
- R nkk , Rekonen P., Kaarniranta K. et al. Matrix metalloproteinases and their inhibitors in the chamber angle of normal eyes and patients with primary open-angle glaucoma and exfoliation glaucoma. Graefe’s Arch Clin Exp Ophthalmol 2007; 245:697-704.
- Schl tzer-Schrehardt , Lommatzsch J., Kuchle M., Konstas A.G., Naumann G.O. Matrix metalloproteinases and their inhibitors in aqueous humor of patients with pseudoexfoliation syndrome/ glaucoma and primary open-angle glaucoma. Invest Ophthalmol Vis Sci 2003; 44:1117-1125.
- Flandin , Buffevant C., Herbage D. A differential scanning calorimetry analysis of the age-related changes in the thermal stability of rat skin collagen. Biochim Biophys Acta 1984; 791:205-211.
- Kronick , Maleef B., Carroll R. The location of collagens with differential thermostabilities in fibrils of bovine reticular dermis. Connect Tissue Res 1988; 18:123-134.Le Lous M., Flandin F., Herbage D., Allain J.C. Influence of collagen denaturation on the chemorheological properties of skin, assessed by differential scanning calorimetry and hydrothermal isometric tension measurement. Biochim Biophys Acta 1982; 717(2):295-300.
- Игнатьева Н.Ю., Данилов Н.А., Лунин В.В. и др. Изменение термодинамических характеристик денатурации коллагена тканей глаз в результате неферментативной гликации. Вестник Московского университета. Химия 2007; 48(2):75-
- [Ignatieva N.Yu., Danilov N.A., Lunin V.V. et al. The change of thermodynamic parameters of collagen denaturation of eye tissues due non-enzymatic glycation. Moscow University Chemistry Bulletin 2007; 48:75-79. (In Russ.)].
- Аветисов С.Э. Близорукость. М., Медицина; 2002; 744 с. [Avetisov E. Blizorukost [Myopia]. Moscow, Meditsina Publ., 2002: 744 p. (In Russ.)].
- Иомдина Е.Н., Тарутта Е.П., Маркосян Г.А. и др. Биомеханические показатели корнеосклеральной оболочки глаза и состояние соединительнотканной системы у детей и подростков с различными формами прогрессирующей миопии. Российская педиатрическая офтальмология 2013; 1:18-23. [Iomdina N., Tarutta E.P., Markosyan G.A. et al. Biomechanical characteristics of the corneoscleral tunic and the state of the connective tissue system in the children and adolescents presenting with various forms of progressive myopia. Russian Pediatric Ophthalmology 2013; 1:18-23. (In Russ.)].
- Иомдина Е.Н., Тарутта Е.П.. Игнатьева Н.Ю. и др. Фундаментальные исследования биохимических и ультраструктурных механизмов патогенеза прогрессирующей миопии. Российский офтальмологический журнал 2008, 3:7-12. [Iomdina N., Tarutta E.P., Ignatieva N.Yu. et al. Fundamental studies of biochemical and ultrastructural mechanisms of progressive myopia pathogenesis. Russian Ophthalmological J 2008; 3:7-12. (In Russ.)].
- Иомдина Е.Н., Арутюнян Л.Л., Игнатьева Н.Ю. Структурнобиомеханические свойства теноновой капсулы глаз пациентов с первичной открытоугольной глаукомой. Глаукома: теории, тенденции, технологии. В кн.: Сборник научных статей XIII международного конгресса. М., 2015; с. 101-103. [Iomdina N., Arutyunyan L.L., Ignatieva N.Yu. Structural and biomechanical properties of Tenon capsule of the in primary open-angle glaucoma. In: Proc. of the XIII international congress “Glaucoma: theory, tendencies, technologies”. Moscow; 2015: 101-103]. (In Russ.)].
- Chiang J., Daimon M., Wang L.H., Hung M.J., Chang N.C., Lin H.C. Association between mitral valve prolapse and openangle glaucoma. Heart 2015; 101(8):609-615. doi: 10.1136/ heartjnl-2014-306198.