Warning: Use of undefined constant name - assumed 'name' (this will throw an Error in a future version of PHP) in /home/art6125750/xn--80afieejgglfpb6a5a4k.xn--p1ai/docs/wp-content/themes/twentyseventeen-child/functions.php on line 47
Warning: Use of undefined constant name - assumed 'name' (this will throw an Error in a future version of PHP) in /home/art6125750/xn--80afieejgglfpb6a5a4k.xn--p1ai/docs/wp-content/themes/twentyseventeen-child/functions.php on line 47
Нейробиология стала ведущим научным направлением офтальмологии-2020 в проекте Catalyst for a Cure
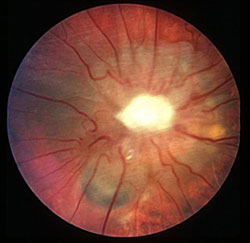
«Ремонт» ганглиев сетчатки – сложнейшая задача. При этом остается неясным, насколько закономерно, тесно и как связаны внутриглазное давление и гибель нейронов
Дорогие друзья,
 Хотелось бы «пробежаться» по материалам, которые мы предлагали вашему вниманию, и выделить самые важные.
Хотелось бы «пробежаться» по материалам, которые мы предлагали вашему вниманию, и выделить самые важные.
Мы уверены: самая важная информация из найденного нами в оригинальных источниках относится к нейродегенерации зрительного аппарата – основной причине необратимой утраты зрения при глаукоме.
Мы обращались к рассказу об этой угрозе неоднократно в течение года; настоятельно предлагаем перечитать вот эти статьи раздела «Актуальное»: http://жизньсглаукомой.рф/act52/; http://жизньсглаукомой.рф/act51/; http://жизньсглаукомой.рф/act40/, а также соответствующие статьи 2018 года: http://жизньсглаукомой.рф/act26; http://жизньсглаукомой.рф/act20/#more-2929 и другие.
Много публикаций на эту тему на информационно-образовательном портале Glaucoma Research Foundations https://www.glaucoma.org/ в разделе архивных материалов https://www.glaucoma.org/gleams/2019/09/.
 Нейродегенерация – термин, описывающий процесс отмирания нейронов, что наблюдается при многих заболеваниях, называемых нейродегенеративными. Нейродегенеративные заболевания – тип заболеваний, особым образом вредящих нервной системе: они вызывают гибель нейронов и, как следствие, дегенерацию нервной ткани
Нейродегенерация – термин, описывающий процесс отмирания нейронов, что наблюдается при многих заболеваниях, называемых нейродегенеративными. Нейродегенеративные заболевания – тип заболеваний, особым образом вредящих нервной системе: они вызывают гибель нейронов и, как следствие, дегенерацию нервной ткани Как мы видели из статьи прошлого месяца, специалисты укрепляются во мнении о том, что именно гибель нервных клеток (нейронов) зрительного нерва, а не повышение внутриглазного давления, фатальна для больного глаукомой.
Именно спасение нейронной сети сетчатки становится сегодня во главу угла у офтальмологов, работающих с глаукомой разной формы и разной степени ее клинической картины.
 Так, доктор Дэвид Калкинс, председатель Научно-консультативного совета (Университет Вандербильт, Теннесси) информирует посетителей портала о том, что каждый аксон (отросток) ганглиозной клетки сетчатки отвечает за обработку визуальной информации в заданной точке сетчатки, а затем за передачу этой информации в мозг через длинное нервное волокно в зрительном нерве. Таких ганглиозных клеток (RGC) в сетчатке каждого глаза человека более миллиона. Когда нервные клетки отмирают, глаза постепенно или спонтанно становятся «отключенными» от мозга, что отражается потерей части поля зрения. Более того, поскольку нервные клетки не регенерируют, утрата зрения необратима.
Так, доктор Дэвид Калкинс, председатель Научно-консультативного совета (Университет Вандербильт, Теннесси) информирует посетителей портала о том, что каждый аксон (отросток) ганглиозной клетки сетчатки отвечает за обработку визуальной информации в заданной точке сетчатки, а затем за передачу этой информации в мозг через длинное нервное волокно в зрительном нерве. Таких ганглиозных клеток (RGC) в сетчатке каждого глаза человека более миллиона. Когда нервные клетки отмирают, глаза постепенно или спонтанно становятся «отключенными» от мозга, что отражается потерей части поля зрения. Более того, поскольку нервные клетки не регенерируют, утрата зрения необратима.
 Хотя понижение глазного давления может помочь замедлить или остановить нейродегенерацию, в настоящее время нет методов лечения для восстановления утраченных нейронов и помощи пациентам, которые уже потеряли зрение.
Хотя понижение глазного давления может помочь замедлить или остановить нейродегенерацию, в настоящее время нет методов лечения для восстановления утраченных нейронов и помощи пациентам, которые уже потеряли зрение.
Проблема реально трудна и еще раз подтверждает, что глаукома представляет собой крайне сложное заболевание. Представим себе, что для «ремонта» ганглиев нужны они сами как «строительный биологический материал», нужны методики их имплантации в сетчатку и поддержание их жизнеспособности на фоне глаукомы. Кроме того, должны формироваться новые сети соединения в сетчатке и отрастать нервные волокна на всем требуемом протяжении.

 Все еще остается открытым вопрос, как и почему определенные нервные клетки теряют свою способность функционировать или «отключают себя». Есть мнение, что разрушающим агентом может выступать повышение внутриглазного давления. В то же время, например, доктор Гарри А. Куигли (Институт медицины Дж. Хопкинса) полагает, что связь внутриглазного давления и гибели ганглиев не столь прямая и однозначная.
Все еще остается открытым вопрос, как и почему определенные нервные клетки теряют свою способность функционировать или «отключают себя». Есть мнение, что разрушающим агентом может выступать повышение внутриглазного давления. В то же время, например, доктор Гарри А. Куигли (Институт медицины Дж. Хопкинса) полагает, что связь внутриглазного давления и гибели ганглиев не столь прямая и однозначная.
 Доктор Джеффри Л. Голдберг, член исследовательской группы Catalyst for a Cure (CFC), придерживается мнения, что актуальны оба этих аспекта и они должны разрабатываться параллельно: «… Аксон ганглиозных клеток сетчатки простирается от сетчатки через зрительный нерв к мозгу, и его проекции повреждаются глаукомой. В дополнение к методам лечения, направленным на снижение глазного давления, которые по-прежнему являются основой терапии глаукомы, могут существовать возможности для разработки новых типов методов лечения, направленных на сетчатку и мозг».
Доктор Джеффри Л. Голдберг, член исследовательской группы Catalyst for a Cure (CFC), придерживается мнения, что актуальны оба этих аспекта и они должны разрабатываться параллельно: «… Аксон ганглиозных клеток сетчатки простирается от сетчатки через зрительный нерв к мозгу, и его проекции повреждаются глаукомой. В дополнение к методам лечения, направленным на снижение глазного давления, которые по-прежнему являются основой терапии глаукомы, могут существовать возможности для разработки новых типов методов лечения, направленных на сетчатку и мозг».
 Конкретно о нейробиологических инновационных методах и результатах мы, вероятно, сможем поговорить уже в наступающем году. Поводы для оптимизма есть. Доктор Эндрю Д. Хуберман говорит: «Моя лаборатория изучает биологию ганглиозных клеток, чтобы определить, какие из них уязвимы на ранних стадиях глаукомы, и как лучше всего их лечить на молекулярном уровне, чтобы сохранить их и не дать им умереть».
Конкретно о нейробиологических инновационных методах и результатах мы, вероятно, сможем поговорить уже в наступающем году. Поводы для оптимизма есть. Доктор Эндрю Д. Хуберман говорит: «Моя лаборатория изучает биологию ганглиозных клеток, чтобы определить, какие из них уязвимы на ранних стадиях глаукомы, и как лучше всего их лечить на молекулярном уровне, чтобы сохранить их и не дать им умереть».
Доктор Хуберман с энтузиазмом относится к возможности помочь поврежденным ганглиям восстановиться: «В конце концов, мы надеемся даже отремонтировать или восстановить часть зрительной системы, если она уже повреждена».

Иллюстрацией нам послужит исследование, выполненное в 2018 г. междисциплинарной группой ученых из нескольких университетов Италии; оригинал текста можно изучить здесь.
Рабочая гипотеза итальянских авторов о сосуществовании болезни Альцгеймера и открытоугольной глаукомы у пожилых людей строилась на лабораторном (частью патологоанатомическом) и литературном материале, выявившем у этих патологий общие черты, факторы риска и патофизиологические механизмы.
Авторы предположили, что у 23-30 процентов общей численности больных глаукомой патогенез глаукомы может быть обусловлен и отягощен иными факторами риска, помимо повышения внутриглазного давления.

Были проанализированы истории болезни (более 100 тысяч) и описана хроника появления в разных странах в 2011-2015 гг. рабочей гипотезы о том, что глаукому в ряде случаев (при стечении обстоятельств патофизиологического характера) можно рассматривать не только как самостоятельное заболевание, но и как часть сложного многофакторного нейродегенеративного процесса, бьющего в том числе по зрению.
Совокупные результаты когерентной томографии зон головного мозга и тканей глаз подтвердили, что у части больных глаукомой (в среднем у 27,5% от общей численности больных открытоугольной формой) в анамнезе действительно повышен риск развития болезни Альцгеймера, даже на фоне физиологической нормы внутриглазного давления.
Однако эти данные офтальмологов и нейробиологов разных стран не всегда согласуются между собой. Особенно сложно интерпретировать их среди пациентов с глаукомой закрытоугольного типа и нормального напряжения, поэтому эти две формы глаукомы временно выведены за рамки исследований данного направления.
Сегодня много аргументов в пользу сходства патогенных механизмов, «запускающих» как болезнь Альцгеймера, так и открытоугольную глаукому.
Например, на патологоанатомических препаратах показано, что зрительные нервы пациентов с глаукомой, с Альцгеймером, и имеющих обе патологии, дегенерированы (лишены аксонов) в равной степени – их в среднем втрое меньше, по сравнению с препаратами, взятыми посмертно у лиц, не страдавших этими патологиями. Более того, погибающие аксоны быстро теряют нормальную плотность. Было продемонстрировано активное разрастание замещающих клеток на месте погибших аксонов у больных глаукомой и/или Альцгеймером.
Предположительно, такие разрушения запускаются нейротоксинами, – уже выделены белковые соединения стекловидных тел и фрагментов поверхности сетчатки, общие для глаукомы и Альцгеймера, так называемые фракции Тау и Аβ-42; изучаются также определенные протеины, глобулины и ретины.
Есть мнение, что при снижении внутричерепного давления в кровоснабжение мозга и глаз вмешиваются упомянутые нейротоксины, вызывая в том числе окислительный стресс тканей и дегенерацию нейронов сетчатки.
Имеет место также гипотеза об изменениях динамики циркуляции спинномозговой жидкости, которую предлагается отслеживать у больных Альцгеймером и глаукомой для синхронной диагностики.
Высказываются гипотезы о формировании дополнительных тканевых образований, способствующих скоплению нейротоксинов в тканях глаз и мозга и препятствующих их выведению.
Интересны предположения о том, что ткани глаза и мозга в случае глаукомы и Альцгеймера теряют одни и те же нормальные клеточные ресурсы жизнедеятельности.
Зоной трагических событий в любом случае оказывается нейрон зрительного нерва как некий стоковый участок.
Есть множество других предположений, их проверка становится задачей будущего.

- Yang Hu, MD, PhD;
- Derek Welsbie, MD, PhD;
- Anna La Torre, PhD,
- Xin Duan, PhD и их коллегам

