Авторы
- Борзунов О. И., ГБОУ ВПО Уральский государственный медицинский университет Минздрава России, кафедра офтальмологии
- Коротких С. А., ГБОУ ВПО Уральский государственный медицинский университет Минздрава России, кафедра офтальмологии
Диабетическая ретинопатия (ДР) и первичная открытоугольная глаукома (ПОУГ) являются основными причинами слепоты, поэтому их сочетание представляет очень серьезный негативный прогноз для пациента. В мире более 60 млн. человек страдают глаукомой, из них, в 72,3‑96,1% — ПОУГ. У 11,7% пациентов глаукома является причиной слепоты на обо их глазах [1,2]. Более 200 млн. человек болеют сахарным диабетом (СД), и около 25 млн. потеряли зрение вследствие его осложнений. В России число больных СД превышает 8 млн. человек [3].
Остается открытым вопрос о риске глаукомного поражения у пациентов с диабетом. В 6‑13% случаев СД диагностируют ПОУГ [4]. Частота ПОУГ не зависит от тяжести заболевания СД. При этом, частота и выраженность ДР зависят от степени компенсации и длительности протекания диабета [3]. Ряд авторов считает, что диабет является отягчающим фактором в патогенезе глаукомного поражения, при этом, приводятся данные, что СД достоверно коррелирует с риском развития двусторонней нормотензивной глаукомы [5]. У пациентов, страдающих СД II типа, глаукома развивается в 4‑5 раз чаще [4].
Наличие СД усложняет лечение ПОУГ по ряду причин: применение β‑блокаторов маскирует симптомы гипогликемии; снижение внутриглазного давления (ВГД) на 20% и более может приводить к ускорению прогрессирования ДР; применение инстилляций простагландинов способствует развитию или усилению диабетического макулярного отека [4].
В то же время, нормализация офтальмотонуса является важнейшим звеном в лечении глаукомы [2,3,6].
Целью исследования явилась оценка офтальмонейропротекторного лечения пациентов с ПОУГ на фоне сахарного диабета II типа в условиях специализированного стационара. Проведен ретро — и проспективный анализ различных вариантов лечения пациентов с сочетанием ПОУГ и СД (II типа).
Задачи исследования: изучение безопасности про ведения селективной лазерной трабекулопластики (СЛТ) пациентам с ПОУГ на фоне риска диабетического макулярного отека; подбор и обоснование наиболее сбалансированной терапевтической стратегии у больных с ПОУГ и СД.
Материал и методы
Исследование проведено на 130 больных (248 глаз), 110 из которых страдали ПОУГ II‑III стадий и 20 человек не имели патологии органа зрения. Пациентами были 76 мужчин (58,5%) и 54 женщины (41,5%) со средним возрастом 68,3±2,3, средней продолжительностью заболевания глаукомой на момент первичного обследования — 7,2±1,3 года, сахарным диабетом — 11,4±2,5 года. Среди сопутствующей внутриглазной патологии отмечено наличие начальной катаракты на 23 глазах (9,3%).
Нейропротекторное лечение проводили после компенсации ВГД. Все пациенты, страдающие сахарным диабетом, параллельно наблюдались у эндокринолога. Лазерное лечение (СЛТ) проводили только на фоне компенсации уровня сахара крови. На момент начала лечения пациенты получали различные варианты местной гипотензивной терапии, но, при этом, имели декомпенсированное ВГД. Критерием исключения из исследования яви лось наличие возрастной макулярной дегенерации, выраженных помутнений оптических сред глаза, неоваскулярной глаукомы, пролиферативной диабетической ретинопатии, миопии III степени, амблиопии.
Кроме того, в исследование не включали пациентов с толщи ной роговицы в центре менее 520 микрон, а также пере несших в течение последних 3 месяцев хирургические и лазерные вмешательства на глазах и имевшие рефракционные операции в анамнезе. Для хирургического вмешательства по поводу глаукомы использовали офтальмологический лазер Laserex Tango (Австралия) и гониолинзу Latina SLT lens (США).
Пациенты были разделены на группы: основную — 40 чел. (77 глаз), группу сравнения I — 37 чел. (71 глаз), группу сравнения II — 33 чел. (60 глаз), группу контроля — 20 человек (40 глаз). В основной группе применяли следующую схему лечения: СЛТ, Ретиналамин® 5 мг парабульбарно № 10; в группе сравнения 1: СЛТ и Ретиналамин® 5 мг парабульбарно № 10, с по следующим лечением препаратом Танакан по 1 таблетке 3 раза в день в течение 3‑х месяцев, в группе сравнения 2: СЛТ, электрическую симпатокоррекцию № 7‑10 (до достижения состояния вегетативного баланса) и Ретиналамин® 5 мг парабульбарно № 10, с последующим лечением препаратом Танакан по 1 таблетке 3 раза в день в течение 3‑х месяцев (табл. 1).
Предложенные схемы лечения (тип и параметры лазерной операции, сочетание групп препаратов и физиотерапевтического лечения) основаны на наших предыдущих исследованиях, касающихся патогенетического лечения первичной открытоугольной глаукомы на фоне симптомов сосудистой дисрегуляции (мигрень, вазоспазм, нейроциркуляторная дистония, состояние симпатотонии, ваготонии) и без таковых [7‑10].
Таблица 1. Характеристика групп исследования
|
Группа |
Основная группа n = 40 (77 глаз) |
Группа сравнения 1 n = 37 (71 глаз) |
Группа сравнения 2 n = 33 (60 глаз) |
Контрольная группа n = 20 (40 глаз) |
|
Характеристика группы |
ПОуГ без симптомов сосудистой дисрегуляции |
ПОуГ на фоне сахарного диабета без симптомов сосудистой дисрегуляции |
ПОуГ на фоне сахарного диабета с симптомами сосудистой дисрегу-
ляции |
Без заболеваний органа зрения и симптомов сосудистой дисрегуляции |
|
Лечение |
СЛТ с последующей нейропротекторной терапией |
СЛТ, нейропротекторная терапия и последующее лечение препаратом Танакан |
СЛТ, симпатокоррекция, нейропротекторная терапия, последующее лечение препаратом Танакан |
Наблюдение в динамике |
Таблица 2. Выраженность гипотензивного эффекта по результатам офтальмотонометрии в различные сроки наблюдения после лазерного гипотензивного лечения (СЛТ) (мм рт. ст.)
|
Срок наблюдения |
Основная группа n = 40 (77 глаз) |
Группа сравнения 1 n = 37 (71 глаз) |
Группа сравнения 2 n = 33 (60 глаз) |
Контрольная группа n = 20 (40 глаз) |
| После лечения (первое наблюдение для группы контроля) |
29,8±1,71 |
28,8±0,79 |
29,9±1,06 |
17,1±1,75 |
| Через 3 мес. |
18,8±0,82* |
19,8±1,46* |
18±0,75* |
17,3±1,67 |
| Через 6 мес. |
19±1,13* |
19,7±1,13* |
18±0,48* |
17,6±1,78 |
| Через 9 мес. |
21,1±0,71* |
22,6±0,97* |
21±0,63* |
18,1±2,01 |
| Через 12 мес. |
22,1±0,39* |
23,8±0,71* |
22,1±0,45* |
17,8±1,74 |
Статистически достоверной разницы между основной группой, группой сравнения I и II в аналогичные сроки наблюдения не выявлено (на уровне р > 0,05). Достоверные различия * — на уровне р<0,05 (по сравнению с данными до лечения).
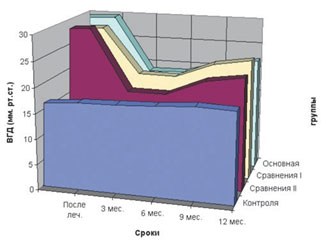
Рисунок 1. Динамика колебаний внутриглазного давления в различные сроки наблюдения
Применяли следующие параметры СЛТ: длина волны — 532 нм; диаметр пятна — 400 мкм; энергия — 0,4‑1,2 мДж (0,4‑0,8 — при пигментированной трабекуле, 0,9‑1,2 — при низко пигментированной трабекуле); длительность — 3 нс, окружность — 270 градусов (3 квадранта, исключая верхний).
Офтальмологическое обследование проводили до и после лечения, затем через 3, 6, 9 и 12 месяцев. Обследование включало: визометрию, авторефрактометрию, биомикроскопию, гониоскопию, офтальмоскопию, тонометрию по Маклакову с определением тонометрического ВГД, пахиметрию для исключения пациентов с тонкой роговицей, компьютерную периметрию (с помощью анализатора Humphrey Visu al Field Analyzer II (HFA II) 750 (Германия) с использованием центрального теста из 76 точек в пределах 30° от точки фиксации (пороговая программа 30‑2, анализируемые параметры — MD (Mean deviation) и PSD (Pattern standard deviation), фотографирование глазного дна (Carl Zeiss Fundus Cam (Германия), оптическую когерентную томографию (SOCT Copernicus (Fundus reconstr. Tomogram 25), оценку порога электрической чувствительности сетчатки и электрической лабильности.
Симпатокоррекцию проводили с помощью аппарата «Симпатокор‑02» (рег. уд. № 29/03051097/1267‑00 от 30.11.2000; ФСР № 2007/00757 от 28.09.2007). Параметры воздействия выбирали в зависимости от тонуса вегетативной нервной системы пациента. Комплексную оценку вегетативного баланса для выявления симптомов сосудистой дисрегуляции выполняли путем анализа вариабельности сердечного ритма с помощью электроэнцефалографа — анализатора «ЭЭГА 21/26 «Энцефалан‑131‑03» (Россия) в условиях покоя, орто и клиностатической пробы, с расчетом уровня вегетативного баланса (соотношение низких и высоких частот — LF/HF).
Отрицательные значения расценивали как ваготонию, положительные — как симпатотонию. Помимо кардиоинтервалографии для исследования состояния вегетативной нервной системы, рассчитывали вегетативный индекс Кердо (до исследования, ежедневно в процессе лечения, в конце всего курса лечения и через 3, 6, 9 и 12 месяцев после лечения). Процедуры симпатокоррекции (№ 5‑10) про водили до достижения уровня вегетативного баланса (0±0,1) [7].
Таблица 3. Динамика клинических показателей в основной группе (после проведения СЛТ)
|
Параметры (M±m) Сроки, подгруппы |
Острота зрения |
Mean Deviation, дБ |
Pattern Standard Deviation, дБ |
ПЭЧ мкА |
КЧ СМ (Гц) |
Площадь НРП (мм2) |
Соотношение площади Э/Д |
|
|
Основная группа (СЛТ + нейропротекторная терапия) |
До лечения |
0,45±0,04 |
–13,3±1,2 |
7,3±0,8 |
196,3±9,3* |
29,2±2,3 |
0,95±0,08 |
0,51±0,15 |
|
После лечения |
0,60±0,06* |
–7,1± 1,3* |
4,6±1,0* |
136,1±9,6* |
37,1±2,3* |
0,95±0,13 |
0,51±0,17 |
|
|
Через 6 мес. |
0,58±0,05* |
–7,9±1.2* |
4,2±1,2* |
142,2±8,6* |
35,3±1,7* |
0,95±0,12 |
0,51±0,17 |
|
|
Через 9 мес. |
0,56±0,03* |
–8,4±0,9* |
4,9±1,9 |
156,5±9,0* |
33,7±2,2 |
0,93±0,11 |
0,61±0,11 |
|
|
Через 1 год |
0,50±0,07 |
–9,6±2,1 |
5,8±1,8 |
187,6±10,2 |
30,4±2,1 |
0,90±0,07 |
0,69±0,11 |
|
|
Группа сравнения I (СЛТ+ нейропротекторная терапия + Танакан) |
До лечения |
0,46± 0,04 |
–13,4±1,2 |
7,4± 0,7 |
201,3± 7,4 |
29,2± 2,3 |
0,98± 0,12 |
0,78± 0,12 |
|
После лечения |
0,60± 0,08* |
–7,7± 1,3* |
4,2±0,9* |
142,7±6,6* |
35,1±2,3* |
0,98±0,15 |
0,78±0,17 |
|
|
Через 6 мес. |
0,57 ±0,05* |
–8,1±1.2* |
4,5±1,1* |
149,1±7,4* |
34,7±1,7* |
0,95±0,15 |
0,51±0,27 |
|
|
Через 9 мес. |
0,56±0,06* |
–8,4±1,9* |
5,3±1,7 |
183,0±8,9 |
31,8±2,2 |
0,93±0,16 |
0,61±0,21 |
|
|
Через 1 год |
0,53±0,07 |
–10,4±2,1 |
6,2±2,1 |
190,2±4,6 |
22,4±2,1 |
0,90±0,12 |
0,69±0,21 |
|
|
Группа сравнения II (СЛТ+ нейропротекторная терапия + симпатокоррекция + Танакан) |
До лечения |
0,45± 0,03 |
–12,4±1,1 |
7,3±0,8 |
206,3±7,4 |
29,1±2,3 |
0,97±0,12 |
0,77±0,13 |
|
После лечения |
0,60± 0,08* |
–7,7± 1,3* |
4,2±0,9* |
142,7±6,6* |
35,1±2,3* |
0,98±0,15 |
0,78±0,17 |
|
|
Через 6 мес. |
0,58 ±0,05* |
–8,1±1.2* |
4,5±1,1* |
149,1±7,4* |
33,7±1,7 |
0,95±0,15 |
0,51±0,27 |
|
|
Через 9 мес. |
0,56±0,06* |
–8,3±1,9 |
5,3±1,7 |
173,0±8,9* |
31,8±2,2 |
0,93±0,16 |
0,61±0,21 |
|
|
Через 1 год |
0,53±0,06 |
–10,3±2,2 |
6,2±2,1 |
191,2±4,6 |
23,2±2,1 |
0,90±0,12 |
0,69±0,21 |
|
|
Группа контроля (Без заболеваний органа зрения и симптомов сосудистой дисрегуляции) |
До лечения |
0,95± 0,14 |
0,4±1,2 |
0,4±0,7 |
50,3±7,4 |
48,2±2,4 |
1,38±0,12 |
0,41±0,13 |
|
После лечения |
0,95± 0,18 |
0,7± 1,3 |
0,2±0,9 |
52,7±6,6 |
47,1±2,3 |
1,48±0,15 |
0,42±0,16 |
|
|
Через 6 мес. |
0,94±0,25 |
0,1±1.2 |
0,5±1,1 |
54,1±7,4 |
49,7±1,7 |
1,35±0,15 |
0,41±0,28 |
|
|
Через 9 мес. |
0,96±0,16 |
0,4±1,9 |
0,3±1,7 |
59,0±3,9 |
49,8±2,2 |
1,33±0,16 |
0,42±0,21 |
|
|
Через 1 год |
0,98±0,17 |
0,4±2,1 |
0,2±2,1 |
54,2±4,6 |
48,4±2,2 |
1,34±0,12 |
0,42±0,23 |
|
Примечание: достоверные различия * — на уровне р < 0,05 до и после лечения.
Сущность терапии с помощью аппарата «Симпатокор‑02» заключается в формировании между многоэлементными электродами, расположенными в проекции шейных ганглиев, пространственно распределенных полей низкочастотных электрических импульсов (частота от (10±5) до (65±10) Гц, длительность — от (100±50) до (400 + 100) мкс, амплитуда — от 0 до 20 В. Для блокирования активности ганглиев симпатической нервной системы, расположенных в области шеи (верхнего шейного и звездчатого), индивидуально для каждого пациента устанавливали значения биотропных параметров импульсов тока [11].
Результаты и обсуждение
Результаты сравнительного исследования динамики внутриглазного давления (ВГД) в различные сроки приведены в таблице 2 и отражены на рисунке 1. Данные основных офтальмологических параметров при ведены в таблице 3.
Рассмотренные в динамике параметры зрительного анализатора доказывают, что в основной группе (СЛТ и Ретиналамин®), группе сравнения I (СЛТ, Ретиналамин® и Танакан) и группе сравнения II (СЛТ, Ретиналамин®, симпатокоррекция и Танакан) отмечено достоверное улучшение остроты зрения и электрофизиологических показателей (p<0,05). Данные стабильности оцениваемых параметров в трех группах оказались схожими, несмотря на наличие диабетической ретинопатии в группах срав нения I и II, а также симптомов сосудистой дисрегуляции в группе сравнения II, что свидетельствует об адекватно подобранном комбинированном лечении [12,13], включающем лазерное гипотензивное лечение, электрическую симпатокоррекцию и введение препарата Ретиналамин.
Таким образом, исследование подтверждает тезис o том, что нейропротекторная терапия глаукомы эффективна только на фоне компенсированного офтальмотонуса. Несмотря на взаимное отягощение анамнеза, ДР и ПОУГ имеют общие компоненты патогене за, в первую очередь, сосудистый компонент, в связи с этим, важным элементом комбинированной терапии является определение тонуса вегетативной нерв ной системы [14,15] и включение электрофизиологической симпатокоррекции в схему лечения, что позволяет добиться стабилизации обоих патологических процессов, избегая полипрагмазии и, как следствие, нежелательных побочных эффектов [13].
Выводы
Селективная лазерная трабекулопластика — метод выбора гипотензивного лечения у пациентов, страдающих сочетанием глаукомы и диабетической ретинопатии.
Эффективной терапевтической стратегией у пациентов с сочетанием первичной открытоугольной глаукомы и сахарного диабета на фоне симптомов сосудистой дисрегуляции является сочетание симпатокоррекции со следующей схемой лечения: Ретиналамин® 5 мг парабульбарно № 10, Танакан по 1 таблетке 3 раза в день — 3 месяца.
Пациентам, имеющим достоверную отрицательную динамику основных офтальмологических параметров показано прохождение курсов консервативного лечения не реже 1 раза в 9 месяцев, в случае выраженного прогрессирования глаукомной оптической нейропатии — вопрос о сроках решается индивидуально.
Литература
- Егоров Е. А. и соавт. Глаукома. Национальное руководство М.: ГЭОТАР — Медиа, 2013.
- Нестеров А. П. Глаукома. Медицинское информационное агентство 2008.
- Аветисов С. Э., Егоров Е. А., Мошетова Л. К. и соавт. Офтальмология: Национальное руководство М.: ГЭОТАР — Медиа, .
- Алексеев И. Б., Мошетова Л. К., Воробьева И. В. Медикаментозная активация увеосклерального оттока у пациентов с глаукомой, протекающей на фоне сахарного диабета. Глаукома 2002; 1: 15‑17.
- Дуюн И. А., Апагуни А. Э., Камфарина И. А. Об эффективности Азопта у пациентов с первичной открытоугольной глаукомой и сахарным диабетом. Клиническая офтальмология. Прилож. к РМЖ 2011; 1: 19‑21.
- Курышева Н. И. Роль методов визуализации диска зрительного нерва и слоя нервных волокон сетчатки в ранней диагностике глаукомы. Глаукома 2007; 1:16‑22.
- Борзунов О. И. Коротких С. А., Кубланов В. С., В. В. Андреева Способ комбинированного лечения открытоугольной глаукомы после лазерной гипотензивной операции. Патент RU 24792902013, 04.13.
- Коротких С.А., Борзунов О.И. Клиническая оценка селективной лазерной трабекулопластики в сочетании с нейропротекторной терапией у пациентов с открытоугольной глаукомой. Уральский медицинский журнал 2010; 10 (75): 131‑133.Борзунов О. И., Коротких С. А., Залесова В. В. Особенности селективной лазерной трабекулопластики (слт) у пациентов с открытоугольной глаукомой в условиях специализированного стационара. Вестник уральской медицинской академической науки 2011; 2 (34):77‑79.
- Борзунов О. И. Оптимизация комбинированного лечения пациентов с открытоугольной глаукомой. Дис. канд. мед. наук. Москва,
- Кубланов B. C. Электрофизический способ коррекции нарушений системы регуляции кровоснабжения головного мозга. Биомедицинская радиоэлектроника 1999; 4:12‑15.
- Klamann M. K., Maier A. K., Gonnermann J. Adverse Effects and Short‑term Results After Selective Laser Trabeculoplasty. Journal Of Glaucoma 2014; 23 (2), 105‑108.
- Ha JH, Bowling B, Chen SD Cystoid macular oedema following selective laser trabeculoplasty in a diabetic patient. Clin Experiment Ophthalmol. 2013; 22: 121‑126.
- Курышева Н. И., Царегородцева М. А., Рябова Т. Я., Шлапак В. Н. Перфузионное давление и первичная сосудистая дисрегуляция у больных глаукомой нормального давления. РМЖ. Клиническая офтальмология 2011; 1: 9‑12
- Бакшинский П. П., Боголюбская А. Ю., Дроздова Г. А. Вайвлет Анализ общей и глазной микрогемодинамики у больных первичной открытоугольной глаукомой с нормализованным внутриглазным давлением. Глаукома 2006; 1: 7‑15

