Авторы
- Д.В. Липатов, доктор мед. наук, заведующий отделением “Диабетическая ретинопатия и офтальмохирургия” ФГУ Эндокринологический научный центр Минздравсоцразвития РФ;
- Т.А. Чистяков, научный сотрудник отделения “Диабетическая ретинопатия и офтальмохирургия” ФГУ Эндокринологический научный центр Минздравсоцразвития РФ;
- А.Г. Кузьмин, научный сотрудник отделения “Диабетическая ретинопатия и офтальмохирургия” ФГУ Эндокринологический научный центр Минздравсоцразвития РФ;
- Ю.В. Баутина, аспирант отделения “Диабетическая ретинопатия и офтальмохирургия” ФГУ Эндокринологический научный центр Минздравсоцразвития РФ;
- М.В. Туховская, аспирант отделения “Диабетическая ретинопатия и офтальмохирургия” ФГУ Эндокринологический научный центр Минздравсоцразвития РФ.
Во всем мире наблюдается лавинообразный рост пациентов с сахарным диабетом (СД). Эксперты ВОЗ расценивают эту ситуацию как эпидемию и говорят о цифре в 350 млн, заболевших к 2025 г. [1]. Особо бурный прирост больных СД (почти в 2 раза) ожидается в Африке и Юго-Восточной Азии, на Среднем Востоке. В Российской Федерации на начало 2010 г. в официальном регистре числилось более 3 млн пациентов с СД, почти пятая часть которых (19,85%) имела проблемы со зрением [2].
С другой стороны, глаукома занимает одно из лидирующих мест среди глазных заболеваний, в большом проценте случаев приводящих к развитию слепоты. Вторичная неоваскулярная (рубеозная) глаукома при СД является одной из наиболее тяжелых форм ее проявления и считается одной из терминальных форм пролиферативной диабетической ретинопатии. По нашим данным [3], она диагностируется у 0,3% пациентов, обратившихся за консультацией к окулисту по поводу глазных проявлений СД.
Новообразованные сосуды радужки характеризуются быстрым ростом, массивной транссудацией плазмы и повышенной ломкостью, которая приводит к возникновению кровоизлияний. В развитии слепоты существенное значение имеет просачивание из новообразованных сосудов белковых фракций плазмы крови, которые запускают процессы рубцевания в тканях сетчатки и стекловидного тела, что в конечном счете может быть причиной тракционной отслойки сетчатки. Неоваскуляризация переднего отрезка глаза приводит к изменению структуры угла передней камеры глаза, нарушению оттока внутриглазной жидкости и развитию вторичной неоваскулярной глаукомы.
В середине 90-х годов ХХ века на “второй волне” развития факоэмульсификации (ФЭ) как во всем мире, так и в России (“первой волной” по праву можно назвать конец 70-х годов ХХ века, когда был выработан сам принцип дробления ядра ультразвуком и сконструированы первые аппараты для ФЭ) был предложен термин – “русская катаракта”.
Сначала к ней относили случаи зрелой и перезрелой катаракты с плотностью ядра хрусталика 4 и 4балла по шкале Буррато, которые требовали длительного использования ультразвука на высокой мощности, что вызывало в послеоперационном периоде стойкий отек стромы роговицы, который иногда заканчивался развитием эпителиально-эндотелиальной дистрофии (ЭЭД) роговицы.
Потом понятие стало собирательным и объединило все случаи так называемой осложненной катаракты – пациентов с ригидным зрачком, задними синехиями, сопутствующей глаукомой в анамнезе, подвывихом хрусталика различной степени и этиологии, симптомами набухания хрусталика, мелкой передней камерой и т.п.
Необходимо сказать о том, что термин “русская катаракта” стал интернациональным, так как им пользовались не только отечественные, но и зарубежные хирурги и врачи-исследователи. Некоторые исследователи предлагают для таких осложненных случаев глаукомы собирательный термин “русская глаукома”.
Под этим названием они предлагают объединить различные варианты протекания вторичной рубеозной глаукомы, которые сопровождаются неоваскуляризацией радужки и угла передней камеры глаза (рис. 1), могут сочетаться со зрелой или перезрелой катарактой (рис. 2), характеризуются стойким некомпенсированным на медикаментозной терапии внутриглазным давлением (ВГД), геморрагическим синдромом – гифемой (рис. 3) или гемофтальмом (рис. 4), ригидным зрачком и задними синехиями, бомбажем радужки (рис. 5) с полным или частичным заращением зрачка, дистрофическими процессами в роговице – отеком стромы, буллами, вплоть до ЭЭД (рис. 6), различной степенью несостоятельности связочно-капсулярного аппарата хрусталика (рис. 7), сочетаться с тракционным синдромом вплоть до отслойки сетчатки (рис. 8). Перечисленные симптомы, сочетаясь с глаукомой, могут быть выявлены обособленно или в комплексе друг с другом.
Так как в своей повседневной работе мы часто встречаемся со всеми перечисленными выше случаями у пациентов с СД, то в связи этим считаем, что более правильно было бы говорить не о “русской”, а о “диабетической” глаукоме. В этом термине могут сочетаться все осложненные случаи вторичной рубеозной глаукомы у пациентов с СД со всеми ее осложнениями.
Все виды диабетической глаукомы характеризуются стойким повышением ВГД и плохо поддается консервативному (медикаментозному) лечению. Назначение монотерапии (β-адреноблокаторы, ингибиторы карбоангидразы, аналоги простагландинов и др.) или комбинированных препаратов в большинстве случаев не оказывает желаемого гипотензивного действия из-за грубых нарушений метаболизма у пациентов с СД.
Поэтому целесообразно выполнение различных хирургических вмешательств. Неперфорирующие операции и классическая синусотрабекулэктомия с базальной иридэктомией не дают стойкого гипотензивного эффекта из-за быстого фиброзирования (“закрытия”) зоны вмешательства. Применяемые в последнее время дренирующие операции (с использованием дренажей различных типов) дают хорошие функциональные результаты и могут быть использованы в лечении.
В связи с этим целью данной работы стала оценка эффективности дренажной хирургии и комбинированного медикаментозного лечения вторичной неоваскулярной глаукомы у пациентов с СД.
Материал и методы
В исследование было включено 45 пациентов (47 глаз), находившихся в отделении “Диабетической ретинопатии и офтальмохирургии” ФГУ ЭНЦ в течение 3,5 лет и прооперированных по поводу вторичной рубеозной глаукомы. Среди них было 25 мужчин и 20 женщин. Средний возраст пациентов составил 65,3 ± 6,5 года. У всех больных был субкомпенсированный СД 2 типа средней тяжести на инсулинотерапии, средняя продолжительность которого составила 14,7 ± 5,1 года.
Средний уровень гликированного гемоглобина до операции был 8,5 ± 1,5%. Дооперационное обследование включало офтальмологические (визометрия, авторефрактометрия, бесконтактная тонометрия, компьютерная периметрия, биомикроскопия, офтальмоскопия, ультразвуковое исследование глаза и фотографирование глазного дна на фундус-камере) и общеклинические (стандартный набор клинических анализов, гликемический профиль, гликированный гемоглобин, исследование функции почек и сердечно-сосудистой системы) методы. Средний уровень ВГД до операции составил 42,8 ± 3,5 мм рт. ст.
У всех пациентов была выполнена антиглаукоматозная дренирующая операция с имплантацией силиконовых дренажей Ахмеда и Мольтено. Клапан Ахмеда был имплантирован 40 пациентам (42 глаз), а клапан Мольтено – 5 пациентам (5 глаз). Клапаны имплантировали по общепринятой методике.
Во время подготовки к оперативному вмешательству было проведено еще одно исследование (с сентября 2009 г. по январь 2011 г.). Было обследовано 32 пациента (15 мужчин и 17 женщин, 34 глаза) с диабетической неоваскулярной глаукомой и СД, которые готовились к оперативному вмешательству по поводу отсутствия компенсации ВГД. Средний возраст пациентов составил 56,8 ± 5,4 года.
У всех больных был субкомпенсированный СД 2 типа средней тяжести на инсулинотерапии, средняя продолжительность которого составила 13,1 ± 2,1 года. Средний уровень гликированного гемоглобина до операции был 9,1 ± 1,7%. Заслуживает внимания тот факт, что при обращении к врачу 31% пациентов для компенсации ВГД использовали монотерапию β-блокаторами, 53% были на комбинированной терапии (β-блокаторы с ингибиторами карбоангидразы или аналогами простагландина F) и 16% не пользовались никакими средствами. Средний уровень ВГД при обращении по данным бесконтактной пневмотонометрии составил 42,7 ± 2,7 мм рт. ст., а по данным тонометрии по Маклакову – 44,1 ± 3,5 мм рт. ст. У этих пациентов была отменена предыдущая гипотензивная терапия и назначен комбинированный препарат Косопт (фирма MSD, США).
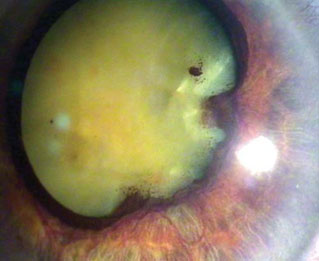
Рис. 1. Рубеоз радужки и угла передней камеры глаза.

Рис. 2. Сочетание со зрелой катарактой.
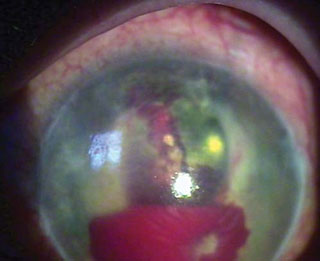
Рис. 3. Сочетание с гифемой.
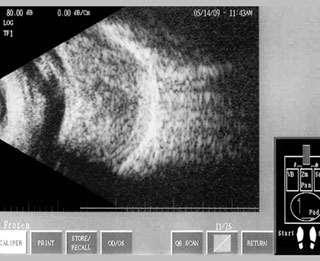
Рис. 4. Сочетание с тотальным гемофтальмом.
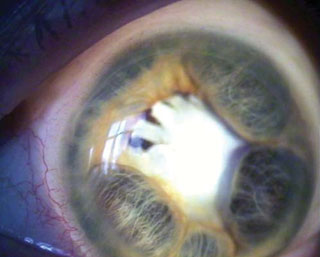
Рис. 5. Ригидный зрачок, задние синехии, бомбаж радужки.
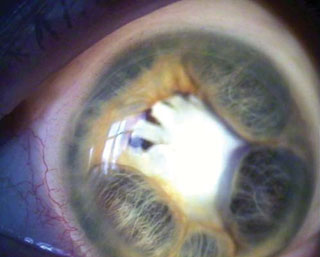
Рис. 6. Изменения в роговице.
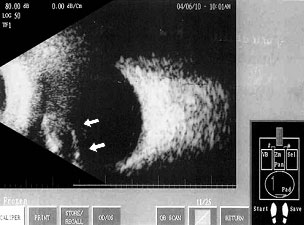
Рис. 7. Сочетание с подвывихом хрусталика.
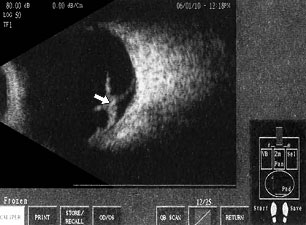
Рис. 8. Сочетание с тракционным синдромом.
Результаты и их обсуждение
У всех пациентов в послеоперационном периоде был купирован болевой синдром и получено стойкое снижение ВГД, которое достоверно отличалось от такового при поступлении. Если исходное ВГД составляло 42,8 ± 3,5 мм рт. ст., то после оперативного вмешательства оно снизилось более чем в 2 раза и составило через неделю после операции 17,9 ± 2,0 мм рт. ст. Последующая динамика изменения послеоперационного уровня ВГД представлена в таблице.
Из-за небольшого количества пациентов (5 глаз) с клапаном Мольтено статистически достоверного различия с данными по клапану Ахмеда в уровне послеоперационного ВГД мы не проводили. Не было получено достоверных данных по различным моделям (FP-7 и FP-8) клапана Ахмеда.
Учитывая тот факт, что модель FP-8 в 2 раза меньше по размеру и более удобна для имплантации (требует меньшего пространства для манипуляций), предпочтение было отдано ей.
В раннем послеоперационном периоде наблюдались следующие осложнения: гифема – у 19 (40%) пациентов, помутнение хрусталика – у 3 (6,4%), уменьшение глубины передней камеры глаза – у 2 (4,2%) пациентов из-за набухания хрусталика. У 1 (2,1%) пациента была диагностирована отслойка сосудистой оболочки, которая не потребовала хирургического вмешательства и была купирована медикаментозными средствами через 5 дней после оперативного вмешательства.
Наличие гифемы в раннем послеоперационном периоде было обусловлено тяжелым исходным состоянием глаз – рубеозные сосуды занимали почти все площадь радужки и угла передней камеры.
Набухание хрусталика и вследствие этого уменьшение глубины передней камеры было обусловлено травматическим воздействием кончика дренажной трубки на переднюю капсулу хрусталика. В дальнейшем длина трубки делалась такой, чтобы всегда быть над радужной оболочкой и не выступать в просвет передней камеры глаза более чем на 2,5–3,0 мм.
В позднем послеоперационном периоде наблюдались следующие осложнения: “захват” радужки – 2 глаза (4,2%), сосудистое бельмо роговицы, ЭЭД роговицы, “обнажение” дренажной трубки – по 1 (2,1%) случаю. Три последних случая вообще можно отнести не к осложнениям данного вида вмешательства, а к особенностям течения диабетической ретинопатии у этих пациентов.
“Захват” радужки отмечался у пациентов с искусственным хрусталиком и, видимо, был обусловлен излишним дренирующим эффектом, при котором существовал отток влаги не только внутри трубки, но и вдоль ее стенки снаружи.
Динамика ВГД в послеоперационном периоде после дренирующих антиглаукоматозных операций
| Показатель |
До операции |
Через 1 нед |
Через 1 мес |
Через 6 мес |
Через 12 мес |
Через 24 мес |
| ВГД, мм рт. ст. |
42,8 ± 3,5 |
17,6 ± 2,1 |
19,3 ± 2,1 |
18,1 ± 1,8 |
17,9 ± 1,7 |
18,0 ± 1,7 |
| Количество глаз (n) |
47 |
47 |
46 |
41 |
29 |
18 |
| р |
<0,05 |
<0,05 |
<0,05 |
<0,05 |
<0,05 |
Использование комбинированного препарата Косопт (фирма MSD, США) дало существенное снижение уровня ВГД (рис. 9) и позволило у 16 пациентов (18 глаз) вообще отказаться от хирургического вмешательства из-за полной нормализации ВГД. У оставшихся 16 пациентов (16 глаз) уровень ВГД также существенно снизился (рис. 10), но не достиг целевого значения, поэтому было принято решение о проведении у них дренирующей антиглаукоматозной операции. У 12 пациентов был имплантирован клапан Ахмеда и у 4 пациентов – клапан Мольтено.
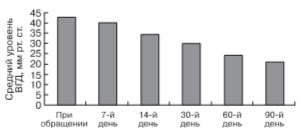
Рис. 9. Динамика среднего уровня ВГД (в мм рт. ст.) при монотерапии Косоптом (n = 34).
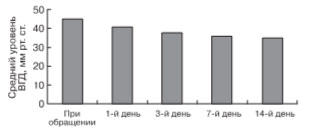
Рис. 10. Динамика среднего уровня ВГД (в мм рт. ст.) у 16 пациентов, которым потребовалось оперативное вмешательство.
Выводы
- Диабетическая глаукома – это не миф, а объективная реальность. Полученные результаты убедительно показывают, что дренажная хирургия диабетической (вторичной рубеозной) глаукомы и ее осложнений должна стать “золотым стандартом” лечения этой патологии у пациентов с СД.
- Диабетическая глаукома – это не миф, а объективная реальность. Полученные результаты убедительно показывают, что дренажная хирургия диабетической (вторичной рубеозной) глаукомы и ее осложнений должна стать “золотым стандартом” лечения этой патологии у пациентов с СД.
- Модернизация существующей методики, исследование и применение различных дренажей, уменьшение травматичности, снижение количества послеоперационных осложнений – основные пути развития дренирующих хирургических вмешательств.
- Использование комбинированных препаратов (например, Косопт фирмы MSD, США) приводит к существенному снижению уровня исходного ВГД и даже в случае отсутствия эффекта (достижение целевого значения) подготавливает глаз пациента к оперативному вмешательству.
Список литературы
- Diabetes Atlas Diabetes Atlas. 2nd еd. IDF 2003.
- Дедов И.И. Новые возможности терапии сахарного диабета 2 типа. Сахарный диабет 2009 (спец. выпуск): 1–3.
- Липатов Д.В., Чистяков Т.А., Кузьмин А.Г. Оценка эффективности дренажной хирургии вторичной рубеозной глаукомы у пациентов с сахарным диабетом: Сборник научных статей “Глаукома: теории, тенденции, технологии”. М.; 2009. 346–351.